Скорость гомогенных и гетерогенных химических реакций зависит от природы реагирующих веществ, концентрации, температуры. Кроме того на скорость химических реакций существенное влияние оказывают физическое состояние реагентов и присутствие катализаторов.
Скоростью гомогенной (гетерогенной) реакции называется количество вещества, вступающего или образующегося в процессе реакции за единицу времени в единице объема (на единице поверхности или на единицу массы или объема твердой фазы). Скорость реакции v обычно характеризуют изменением концентрации с какого-либо из исходных или конечных продуктов реакции в единицу времени r, моль/см3*мин:с2
v = 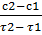 =
= 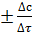
Мгновенная скорость гомогенной реакции v = 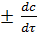 . Если речь идет об убыли концентрации исходного вещества (с2-с1) в интервале времени (
. Если речь идет об убыли концентрации исходного вещества (с2-с1) в интервале времени ( 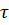 2-
2- 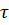 1), то (с2-с1)<0. Скорость есть величина положительная, и в этом случае она берется со знаком минус. Если исходить из концентрации конечного продукта, то (с2-с1)>0 и знак скорости положительный.
1), то (с2-с1)<0. Скорость есть величина положительная, и в этом случае она берется со знаком минус. Если исходить из концентрации конечного продукта, то (с2-с1)>0 и знак скорости положительный.
Согласно закону действующих масс скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях, равных стехиометрическим коэффициентам. Следовательно, в общем виде для реакции, идущей по уравнению
аА + bВ = сС + dD ,
кинетическое уравнение этого закона имеет вид
V=k[А]а*[В]b
При расчете скорости реакции в зависимости от температуры можно пользоваться формулой (правило Вант-Гоффа)
Vt2 = Vt1 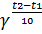
Где Vt2 и Vt1 – скорости реакций при соответствующих температурах; γ- температурный коэффициент реакции, т.е. число, характеризующее увеличение скорости реакции при нагревании системы на 100. Для большинства реакций при обычных условиях γ принимает значения от 2 до 4.
Не все столкновения молекул ведут к их взаимодействию. Чтобы произошла реакция, сталкивающиеся молекулы должны обладать энергией, превышающей среднее значение энергии всех молекул. Такие молекулы называют активными. Энергию, необходимую для активирования молекул, называют энергией активации данной реакции. Энергия активации выражается в кДж/моль. Чем больше энергия активации, тем меньше активных молекул при данной температуре и тем медленнее идет реакция.
От энергии активации зависит также температурный коэффициент скорости реакции γ. Значения его 2,3,4 при обычных температурах соответствуют энергии активации 60,90 и 120кДж/моль. С повышением температуры увеличивается число результативных столкновений молекул и уменьшается энергия активации.
Выполнение неравенства ∆G0<0 не является гарантией фактического течения процесса в данных условиях, и этого не достаточно для оценки кинетических возможностей реакции. Часто для осуществления процесса необходим катализатор, который снимает кинетический «тормоз», и тогда проявляется термодинамическая природа реагирующих веществ.
Пример 1. Во сколько раз изменится скорость прямой и обратной реакции в системе 2SO2(г) + О2(г) ↔ 2SO3(г), если объем газовой смеси уменьшить в три раза? В какую сторону сместится равновесие системы?
Решение. Согласно закону действия масс, выражения скорости прямой и обратной реакции до изменения объема имеют вид
V1 = K  [SO2]2
[SO2]2  [O2]; V = К
[O2]; V = К  [SO3]2
[SO3]2
Где К и К константы скорости соответственно прямой и обратной реакции.
После уменьшения объема гомогенной системы в три раза концентрация каждого из реагирующих веществ увеличится в три раза, тогда: [3SO2], [3О2] и [3SO3]. При новых концентрациях скорости прямой и обратной реакции следующие
V2 = К  [3SO2]2
[3SO2]2 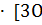 2] = 27К
2] = 27К 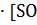 2]2
2]2 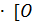 2]
2]
V2 = К  [3SO3]2 = 9K
[3SO3]2 = 9K  [SO3]
[SO3]
Отсюда 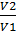 =
= 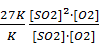 = 27;
= 27; 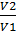 =
= 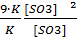 = 9
= 9
Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной – только в 9 раз. Равновесие системы сместилось в сторону образования оксида серы(VI).
Пример 2. Вычислите, во сколько раз увеличится скорость реакции, протекающей в газовой фазе, при повышении температуры от 30 до 700С, если температурный коэффициент реакции равен 2.
Решение. Зависимость скорости химической реакции от температуры определяется эмпирическим правилом Вант-Гоффа по формуле
Vt2 =Vt1 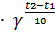
Отсюда имеем
Vt2 = Vt1 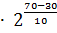 = Vt2
= Vt2  24=16
24=16  Vt1
Vt1
Следовательно, скорость реакции Vt2, протекающей при температуре 700С, увеличилась, по сравнению со скоростью реакции Vt1,протекающей при температуре 300С, в 16раз.
Пример 3. Обратимая эндотермическая реакция разложения хлорида фосфора (V) протекает по уравнению
PCl5(г) = PCl3(г) + Cl2(г); ∆Н0=+92,59кДж
Как надо изменить: а) температуру; б) давление; в) концентрацию, чтобы сместить равновесие в сторону прямой реакции – разложения PCl5?
Решение. Смещением или сдвигом химического равновесия называют изменение равновесных концентраций реагирующих веществ в результате изменения одного из условий реакции. Направление, в котором сместилось равновесие, определяется по принципу ЛеШателье: если на систему в состоянии истинного равновесия воздействовать извне, изменяя термодинамические параметры, то равновесие сместится в таком направлении, которое ослабит эффект приложенного внешнего давления. Таким образом, при изменении температуры, давления и концентрации в рассматриваемой системе наблюдается следующее:
а) так как реакция разложения PCl5 эндотермическая (∆Н0>0), то для смещения равновесия в сторону прямой реакции нужно повысить температуру;
б) так как в данной системе разложения PCl5 ведет к увеличению объема (из одной молекулы газа образуются две газообразные молекулы), то для смещения равновесия в сторону прямой реакции надо уменьшить давление;
в) смещения равновесия в указанном направлении можно достигнуть как увеличением концентрации PCl5, так и уменьшением концентрации PCl3или Cl2.
76. Как повлияет повышение давления при неизменной температуре на равновесие следующих систем:
а) 2HBr ↔ H2 + Br2; ∆Н0 = +72,45 кДж;
б) 2СО + О2 ↔ 2СО2; ∆Н0 = -566,49 кДж;
в) N2 + О2 ↔ 2NO; ∆Н0 = +181,01кДж.
77.Напишите выражение скорости химической реакции,. Протекающей в гомогенной системе по уравнению 3А + 2В = А3В2, и определить, во сколько раз увеличится скорость этой реакции, если : а) концентрация [А] увеличится в два раза; б) концентрация [В] увеличится в три раза; в) концентрация обоих веществ увеличится в два раза.
78. Во сколько раз следует увеличить давление, чтобы скорость образования диоксида азота по реакции 2NO + О2 = 2NO2 возросла в 1000 раз? Ответ подтвердите соответствующими расчетами.
79. Как изменится скорость реакции, протекающей в газовой фазе при повышении температуры на 600С, если температурный коэффициент скорости данной реакции равен γ=3,5?
80. Почему при изменении давления смещается равновесие системы
N2 + 3H2 = 2NH3
и не смещается равновесие в системе
N2 + O2 = 2NO?
Напишите выражения для констант равновесия каждой из данных систем.
81.При некоторой температуре в системе
2NO2(г)↔2NO(г) + О2(г)
константа химического равновесия составляет К=12,8, а равновесная концентрация кислорода [О2] = 0,2 моль/л. Определите начальную концентрацию диоксида азота.
82.Вычислите равновесные концентрации водорода из йода в реакции
Н2 + J2 ↔ 2HJ,
если их начальные концентрации составили по 0,03 моль/л, а равновесная концентрация йодоводорода [HJ] = 0,04 моль/л. Вычислите константу химического равновесия.
83.Почему при изменении давления смещается равновесие системы
2SO2(г) + О2(г) ↔ 2SО3(г)
и не смещается равновесие системы
N2 + O2 ↔ 2NO
Напишите выражение для константы равновесия каждой из данных систем.
84. В каком направлении произойдет смещение равновесия системы
Н2 + S ↔ H2S ,
если: а)увеличить концентрацию водорода; б) понизить концентрацию сероводорода? Составьте выражения скорости прямой и обратной реакций.
85.В каком направлении произойдет смещение равновесия системы
3Fe + 4Н2О ↔ 4Н2 + Fe3О4,
если: а) увеличить концентрацию водорода; б) уменьшить концентрацию паров воды?
86.Вычислите, во сколько разуменьшится скорость реакции, протекающей в газовой фазе, если понизить температуру от 120 до 800С. Температурный коэффициент скорости реакции равен трем.
87.Рассчитайте, как изменятся скорости прямой и обратной реакций в равновесной системе
2С2Н6(г) + 7О2(г) ↔ 4СО2(г) + 6Н2О(г)
если давление увеличить в 3 раза? В каком направлении сместится равновесие?
88.На сколько градусов нужно повысить температуру, чтобы скорость реакции возросла в 90 раз? Температурный коэффициент скорости реакции равен 2,7.
