Из ионов одинакового заряда максимальной способностью к адсорбции обладают ионы наибольшего радиуса (кристаллографического) из-за их меньшей гидратации.
Поясним это:
Молекулы растворенного вещества, растворяясь в воде, распадаются на ионы, которые находятся в гидратированном состоянии.
Рассмотрим ионы первой основной группы (щелочных металлов):
Li+ Na+ K+
Рис.2.38. Примеры размеров ионов в гидратированном состоянии
Ионы одного заряда, но, естественно, разного ионного (кристаллогарфического) радиуса: у Li+ — порядковый номер 4, у Na+ — 23, у K+ — 39, но ионы в воде находятся в гидратированном состоянии, окруженными молекулами (диполями) воды — так называемой «гидратной» оболочкой — «гидратной шубой».
Поскольку плотность поверхностного заряда у ионов разная, то и толщина этой оболочки также будет отличаться, причем у иона меньшего радиуса — (Li+) она будет больше, чем у иона большего радиуса, поэтому радиус ионов в гидратированном состоянии обратен их кристаллографическому радиусу.
По возрастающей адсорбционной способности ионы одного заряда можно расположить в так называемые лиотропные ряды. Рассмотрим некоторые из них:
Li+ < Na+ < K+ < Rb+ < Cs+ Mg+2 < Ca+2 < Sr+2 < Ba+2
В случае анионов, следует учитывать их более сложное строение: ионы могут состоять из нескольких элементов, но и в этом случае гидратированный радиус определяет для ионов одинакового заряда адсорбционную способность ионов.
Рассмотрим ряд однозарядных ионов:
Cl— < Br— < NO3— < J— < CNS—
2. Адсорбция ионов зависит от заряда:
Чем больше заряд, тем больше адсорбция: K+ << Ca+2 << А l+ 3
В очень сильной степени адсорбционная способность ионов возрастает с увеличением их заряда. Вклад заряда в адсорбционную способность ионов преобладает над влиянием их размера. Так, ионы Ва2+ адсорбируются сильнее, чем ионы Rb+, не смотря на то, что радиус последних больше (1,34A0 и 1,47А0, соответственно).
3. Правило Панета — Фаянса(**).
Особый интерес представляет адсорбция ионов поверхностью кристалла, в состав которой входят ионы той же природы. При этом адсорбцию можно рассматривать как кристаллизацию, т.е. достройку кристаллической решетки адсорбированными ионами.
Согласно правилу Панета — Фаянса:
Кристаллы достраиваются лишь теми ионами, которые входят в их состав, а также ионами, изоморфными с ионами кристаллической решетки
Ионно-обменная адсорбция
Адсорбция в растворах-электролитах имеет огромное значение в окружающей нас природе. Именно адсорбция ионов почвой обуславливает её плодородие, а следовательно - и жизнь на Земле.
При адсорбции ионов часто наблюдают так называемую обменную адсорбцию. Она заключается в том, что твёрдый адсорбент поглощает из раствора-электролита катионы или анионы, выделяя одновременно в раствор эквивалентное количество других катионов или анионов.
Сорбенты, способные к обмену ионов, называют ионообменниками или ионитами. Иониты, обменивающиеся с раствором катионами, - катиониты,а обменивающиеся анионами - аниониты.
Амфотерные иониты способны обмениваться как катионами, так и анионами. К катионитам следует отнести алюмосиликаты (цеолиты, пермутиты), силикагель, целлюлозу и т.д.
Примером анионитов могут служить гидроксиды алюминия и железа. Амфотерные иониты способны обменивать и катионы, и анионы. Это синтетические материалы, имеющие состав типа Н+SO3- - R или R – N+(CH3)3OH-, где R – органическая полимерная основа.
 Иониты широко применяются в практической деятельности, особенно их значение возросло после 1935 г, когда был осуществлён промышленный синтез разнообразных искусственных ионообменников – ионообменных смол.
Иониты широко применяются в практической деятельности, особенно их значение возросло после 1935 г, когда был осуществлён промышленный синтез разнообразных искусственных ионообменников – ионообменных смол.
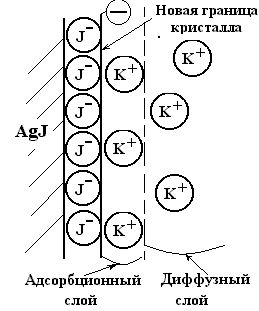
Ионообменные смолы – это высокомолекулярные нерастворимые в воде соединения, способные набухать, поглощая при этом значительное количество воды. При набухании происходит диссоциации их поверхностных полярных групп и в приповерхностном слое ионита образуется ДЭС.
Ионы ДЭС как раз и обмениваются на другие ионы, имеющие большую адсорбционную способность.
Процесс ионного обмена обратим, и его направление зависит от концентрации обменивающихся ионов. Б.П. Никольский и Е.Н. Гапон(**) для описания закономерностей ионного обмена (1939 г) предложили уравнение:
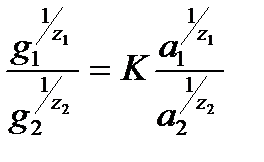 , (2.113)
, (2.113)
где g1 и g2 – содержание обменивающихся ионов в адсорбенте, моль/г; а1 и а2 – активности обменивающихся ионов в растворе; z1 и z2 – заряд ионов; К – константа. При малых концентрациях растворов-электролитов вместо активностей можно использовать концентрации. В этом случае уравнение Никольского – Гапона для однозарядных ионов имеет вид:
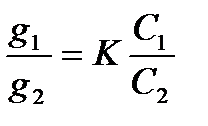 (2.114)
(2.114)
Ионообменная адсорбция на синтетических ионитах часто применяется для деминерализации воды в теплосиловых установках. Довольно широкое распространение она нашла и в пищевых технологиях. Так, в молочной промышленности ионитная обработка молока применяется для получения детского питания, высококачественного легкорастворимого сухого молока и хорошего сгущенного молока (без характерной при избытке кальция “песчаности” и “мутности”). Возможно применение ионитов и для удаления из молока радиоактивных элементов и ионов тяжелых металлов.
Анионитная обработка фруктовых соков позволяет удалять из них кислоты, имеющие неприятный вкус, например яблочную кислоту, и заменить их другими. В производстве лизина микробиологическим путем есть стадия извлечения катионной формы препарата из раствора. Она основана на ионообменной адсорбции:
Обменная адсорбция имеет большое значение для земледелия, так как от природы поглощённых почвой катионов зависит её плодородие. Например, почва способна поглощать и удерживать катионы К+ и NH4+, содержащиеся в удобрениях и необходимые для питания растений. Взамен этих катионов почва выделяет эквивалентные количества других катионов, например Са2+ и Mg2+ Анионы, как, например, С1-, NO3-, SO42-, почти не поглощаются почвой. От природы поглощенных ионов в значительной мере зависят физические и агротехнические свойства почвы.
Иониты широко применяют при получении в производственных условиях деминерализованной воды, т. е. воды, не содержащей растворенных солей (так устраняют жёсткость воды). Для умягчения воды её последовательно пропускают через катионитовый и анионитовый фильтры. Катионит содержит способный к обмену Н+ (Н-форма катионита), анионит – ОН- (ОН - форма анионита).
Рассмотрим в качестве примера удаление NaCI из воды. Катионит, взаимодействуя с хлоридом натрия, обменивает ион натрия на ион водорода, который поступает в раствор:
RH (т) + NaCI (р) Þ RNa (т) + НС1 (р)
Далее воду обрабатывают анионитом в ОН - форме, при этом поглощаются хлорид - ионы:
R'OH (т) + НС1 (р) Þ R'Cl (т) + Н2О,
где RH и R'OH представляют собой иониты, способные к обмену катионов или анионов соответственно.
После использования иониты могут быть регенерированы обработкой раствором серной или соляной кислот (катионит) или растворами гидроксида натрия или гидрокарбоната натрия (анионит).
Большое значение имеют иониты в деле охраны окружающей среды. Так, например, в сточных водах многих производств содержатся ионы тяжелых металлов, которые вредны для живых организмов. Так как концентрация тяжелых металлов в сточных водах очень мала, применение обычных методов очистки (например, осаждения) неэффективно и дорого. Сточные воды пропускают через слой катионита, причем можно использовать катионит, способный обменивать не ионы водорода, а, например, ионы натрия. Ионы тяжелых металлов, обмениваясь на ионы натрия, поглощаются катионитом, из которого их можно извлечь и использовать далее в народном хозяйстве.
Лекция 6
Смачивание. Адгезия. Когзия
Понятия смачивания, адгезии, когезии, растекания относятся к межфазным взаимодействиям, которые наблюдаются между конденсированными фазами.
Адгезия. Когзия
Адгезия — межфазное взаимодействие конденсированных тел разной природы (прилипание).
Адгезия может возникнуть между ж1/ж2, ж/т, т1/т2 (в этом случае одна из фаз была ранее в жидком состоянии). Адгезия — результат стремления системы к уменьшению поверхностной энергии, поэтому адгезия — самопроизвольный процесс при соответствующих условиях.
Адгезия характеризуется работой адгезии — Wa.
Работа адгезии характеризует прочность связи и численно равна работе обратимого изотермического разрыва адгезионного соединения единичной площади.
Полная работа адгезии Ws= WaS (2.115)
Получим соотношение между работой адгезии и поверхностным натяжением взаимодействующих компонентов.
Представим себе 2 контактирующие фазы в конденсированном состоянии, имеющие на границе раздела с воздухом единичную площадь S =1 (2 ж1/ж2 или ж/т) — процесс, обратный рассмотрению образования поверхностного натяжения:
σж/г σт/г
+ 2
3 σт/ж
Рис.2.39. Образование адгезионного соединения
∆G=Gкон - Gнач = σт/ж - σж/г - σт/г (2.116)
Согласно термодинамике полезная работа (в нашем случае Wa) совершается за счет убыли энергии, поэтому Wa = - ∆G, поэтому
Wa = σт/г + σж/г - σт/ж — уравнение Дюпре(*)(2.117)
Из уравнения Дюпре следует, что чем больше работа адгезии, тем меньше sтж. Действительно, чем сильнее межмолекулярные взаимодействия жидкости и твердого тела, тем меньше нескомпенсированность сил в их поверхностном слое и тем меньше межфазное натяжение sтж.
От работы адгезии надо отличать понятие адгезионной прочности Wп — работы разрушения соединения : Wп= Wa+ Wдеф
Wдеф — может быть очень велика и отличаться от Wa в n раз.
Когезия— внутрифазное взаимодействие, обусловленное силами межмолекулярного притяжения различной природы, характеризуется работой когезии Wк.
Работа когезии Wк определяется величиной обратимой изотермической работы разрыва тела по сечению единичной площади.
При обсуждении понятия поверхностного натяжения мы говорили, что эта величина характеризует межмолекулярное взаимодействие внутри фазы и равна работе образования площади, равной единице.
При разрыве тела образуется 2 единичных площади, поэтому
Wк=2 σж/г (2.118)
Когезия отражает межмолекулярное взаимодействие и характеризуется такими параметрами, как Е парообразования, Ткип, Е крист.решетки и т.д.
Механизм процесса адгезии
Процесс адгезии делят на 2 стадии:
1) диффузионная (транспортная) молекул адгезива к поверхности субстрата и их ориентация в пространстве.
Увеличить скорость можно за счет ↑Е, Т, Р, перевода адгезива в жидкое состояние растворением или плавлением.
2) непосредственное взаимодействие адгезива и субстрата за счет различных сил взаимодействия — В-д-В., хим., электростат. и т.д. Ковалентные связи действуют на расстоянии, меньшем 0,5 нм, ионные и В-д-в на r=1 - 100 нм. Контакт возможен, поэтому только при взаимодействии жидких фаз.
