Энергия Гельмгольца
Работа процесса в общем случае, как это уже говорилось, зависит от пути процесса. Работа неравновесного процесса меньше, чем работа равновесного процесса, протекающего между теми же начальным и конечным состояниями системы. В самом деле, исходя из уравнения первого закона термодинамики (I, 2) и уравнения (II, 2), получаем в общем случае:
δW = dQ — dU £ TdS — dU (III, 1)
Величина правой части этого уравнения не зависит от того, равновесен или неравновесен процесс. В случае равновесного процесса:
dW = dWравн. = TdS — dU (III, 1а)
Для неравновесного процесса:
dW < TdS — dU (III, 1б)
Сравнивая уравнения (III, 1а) и (III, 1б), получаем:
dWравн. > dW
Таким образом, работа равновесного процесса максимальна.
Максимальная работа не зависит от пути, а определяется лишь начальным и конечным состояниями системы. Так, при S = const (равновесный адиабатный процесс)
dW = –dU и Wмакс. = U1 – U2
т. е. величина максимальной работы определяется изменением внутренней энергии системы.
Интегрируя при постоянной Т уравнение (III, 1а), получаем:
Wмакс. = T (S2 – S1) – (U2 — U1) (III, 2)
или
Wмакс. = (U1 — TS1) — (U2 — TS2) (III, 2а)
Выражения, стоящие в скобках, являются функциями состояния системы. Введя в уравнение (III, 2а) обозначение
F º U — TS (III, 3)
получаем (при T = const)
Wмакс. = F1 – F2 = –DF (III, 4)
где F — функция состояния, называемая энергией Гельмгольца. Таким образом, максимальная работа при изохорно-изотермических равновесных процессах равна убыли энергии Гельмгольца системы.
Переписав уравнение (III, 3) в виде
U = F + TS
можно рассматривать внутреннюю энергию, как состоящую из двух частей - свободной энергии F и связанной энергии TS. Лишь часть внутренней энергии - свободная энергия, которую система отдает вовне при T = const, может превратиться в работу (условием для такого превращения является равновесность процесса; в неравновесном процессе свободная энергия частично или полностью переходит в теплоту). Другая часть внутренней энергии - связанная энергия - при изменении системы при Т = const не дает работы, а переходит только в теплоту:
Энтропия есть, таким образом, фактор емкости связанной энергии.
Для процессов, протекающих с изменением температуры (T 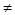 const), деление внутренней энергии на свободную и связанную не может быть проведено и, следовательно, сами термины не имеют общего значения. Поэтому будем пользоваться для функции F названием энергия Гельмгольца.
const), деление внутренней энергии на свободную и связанную не может быть проведено и, следовательно, сами термины не имеют общего значения. Поэтому будем пользоваться для функции F названием энергия Гельмгольца.
Полный дифференциал функции F можно получить, дифференцируя уравнение (III, 3):
dF º dU – TdS – SdT (III, 5)
Сопоставив это уравнение с уравнениями (III, 1а) и (III, 1б), получим в общем виде:
dF £ -SdT – dW (III, 5а)
Откуда при Т = const
(dF)T £ –dW (III, 6)
или
F2 — Fl = DF < —W; Fl — F2 > W (III, 6a)
Выражение (III, 6a) отражает уже известное нам положение, что работа неравновесного процесса меньше работы равновесного процесса.
Если при равновесном процессе совершается только работа расширения (dW = PdV), то из уравнения (III, 5а) получаем:
dF = —SdT — PdV (III, 7}
Это выражение является полным дифференциалом функции F при переменных V и Т.
Полагая T = const и V = const, а также при условии отсутствия всех видов работы (dW = 0), получаем из уравнения (III, 5а):
( 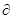 F)V, T £ 0
F)V, T £ 0
т. е., энергия Гельмгольца системы, находящейся при постоянных V и Т не изменяется при равновесных процессах, при неравновесных процессах ее значение убывает.
Так как система, в которой протекают (и могут протекать) только равновесные процессы, бесконечно близка к равновесию, то сформулированные свойства энергии Гельмгольца позволяют судить о том, находится ли данная система в равновесии или нет. В последнем случае направление неравновесного процесса определяется убылью энергии Гельмгольца при постоянных температуре и объеме системы.
Условия, которым должны удовлетворять процессы, для того чтобы по изменениям величины F можно было судить о направлении этих процессов, иные, чем для энтропии. Для энтропии это были условия постоянства внутренней энергии и объема (изолированная система), для энергии Гельмгольца это условие постоянства объема и температуры - легко измеримых параметров системы. Энергия Гельмгольца, являясь производным понятием по отношению к энтропии, представляет собой практически более удобный критерий направления процессов, чем энтропия.
Изложенные соображения могут быть выражены следующим положением: энергия Гельмгольца системы, находящейся при постоянных объеме и температуре, стремится уменьшиться при неравновесных (самопроизвольных) процессах. Когда она достигает минимального значения, совместимого с данными V и Т, система приходит в состояние равновесия.
Энергия Гиббса
Желая учесть в общей форме другие виды работы, кроме работы расширения, представим элементарную работу как сумму работы расширения и других видов работы:
 dW = PdV + dW' (III, 8)
dW = PdV + dW' (III, 8)
где dW' — сумма элементарных работ всех видов, кроме работы расширения. Мы назовем эту величину элементарной полезной работой, а величину W' — полезной работой. Из уравнений (III, 8) и (III, 1) получаем:
dW' £ TdS — dU — PdV (III, 9)
Отсюда можно найти величину W', получаемую при переходе системы из состояния 1 в состояние 2, интегрируя это уравнение в соответствующих пределах при постоянных температуре и давлении:
Сгруппировав все величины, относящиеся к одному состоянию, получим:
W' £ (U1 — TS1+ PV1) — (U2 — TS2 + PV2)(III, 10)
Обозначим через G выражения, стоящие в скобках правой части уравнения, которые являются функциями состояния, т. е.
G º U — TS + PV º H —TS (III, 11)
Тогда уравнение (III, 10) можно записать следующим образом:
W' £ G1 — G2 = —DG (III, 10а)
Так как DG не зависит от пути процесса, то, при условии постоянства P и Т, для равновесных процессов W' будет максимально:
W'макс. = G1 — G2 = — DG (III, 12)
где G - функция состояния, определяемая равенством (III, 11) и называемая энергией Гиббса. Таким образом, максимальная полезная работа при изобарно-изотермических процессах равна убыли энергии Гиббса.
Для получения полного дифференциала функции G при переменных P и Т дифференцируем уравнение (III, 11):
dG = dU — Т dS — SdT + PdV + VdP
Так как
dU £ TdS — PdV— dW',то
dG £ —SdT + VdP — dW' (III, 13)
Из этого уравнения при постоянных Т и P получаем уравнение (III, 10а) в дифференциальной форме.
При отсутствии всех видов работы, кроме работы расширения (dW' = 0), в общем случае:
dG £ —SdT + VdP (III, 13а)
а для равновесных процессов
dG = —SdT + VdP (III, 13б)
Энергия Гиббса системы при постоянных P и Т уменьшается при неравновесных (самопроизвольных) процессах, при равновесии ее значение остается постоянным. Очевидно, равновесное состояние системы при данных P и Т соответствует минимуму энергии Гиббса.
