Внутренняя энергия. Энтальпия. Теплота и работа – две формы передачи энергии.
Внутренняя энергия (U)- зависящая от термодинамического состояния системы, равна сумме всех видов энергии частей системы, за исключением кинетической и потенциальной энергии как целого.
[U]=Дж
Зависит от :
Характера движения и взаимодействия частиц в системе
От природы составляющих систему в-в
От массы
От внешних условий- темп, давл, объема
Энтальпия-энергия, которой обладает система при постоянном давлении
[H]=Дж
Связь энтальпии с внутр энергией ∆H=∆U+A, A=p*∆V
=>∆H=∆U+ p*∆V
А-работа, совершаемая против дей-я внеш сил, р-давление
Стандартная энтальпия-это изменение 1 моля в-ва в стандартных условиях(Т=298К, р=101,325 кПа)
[∆H 0298]=кДж/моль
Расчет изменения энтальпии в процессе хим р-ции
∆H 0298(р-реакции)= ∑n∆H 0298(обр-образования)- ∑n∆H 0298(обрахования исзодных в-в)
Теплота и работа-не форма энергии, а способ ее передачи. Они не являются термическими состояниями, следовательно их величины зависит от пути процесса в отличие от U,H.G,S,F
[Q]=[A]=Дж
3. Первое начало термодинамики: формулировки, применение к биосистемам.
Первое начало термодин=частный случай закона сохря в-вв
Вечный двигатель 1го рода невозможен, т.е. невозможно создать машину, которая производила бы без подведении энергии из вне,иначе говоря «создавать энергию»
Кол-во теплоты, полученное термодинамич-й системой расходуется на увеличение внутр и внеш энергии работы, совершаемую против действия внеш сил.
Q=∆U+A, преобразовав получим ∆U= Q-А
U-внутр энергия
Q-кол-во теплоты
А- работа,совершаемая против действия внеш сил.
Применение к биосистема.Живой организм не явл-ся источником новой энергии, поэтому полностью подчиняется требованиям 1го закона ТД, со следующей формулировкой: Все виды работ в организме совершаются за счет эквивалентного кол-ва энергии, выделяющийся при окислении хим в-в(3я формулировка)
Закон Гесса: формулировка, следствия, практическое значение
Закон Гесса- основной закон термохимии, который формулируется следующим образом:
Тепловой эффект реакции зависит только от природы и состояния исходных веществ и конечных продуктов и не зависит от пути, по которому реакция протекает.
Закон открыт русским химиком Г.И.Гессом в 1840г.
Практическое значение закона Гесса состоит в том, что он позволяет рассчитывать тепловые эффекты самых разнообразных химических процессов; для этого обычно используют ряд следствий из него.
Следствия из закона Гесса:
ü Тепловой эффект реакции равен сумме теплот образования продуктов реакции минус сумма теплот образования исходных веществ
ΔН=∑ΔНпрод.-∑ ΔН исх.
ü Теплота (стандартная энтальпия) образования органического соединения равна разности между теплотой сгорания простых веществ, из которых оно может быть получено ( С-графит, Н2-газ, S-ромб), и теплотой сгорания самого соединения.
ΔН=∑ΔНсгор.исх.-∑ ΔНсгор.прод.
Второе начало термодинамики: формулировки Клаузиуса и Томсона. Свободная и связанная энергия.
Второй закон устанавливает, что все реальные самопроизвольно идущие процессы являются необратимыми
Примеры необрат процессов-расширение газов, растворение, все процессы в организме
Формулировки:
Тепло не может самопроизвольно переходить от более холодного к более тёплому телу (Р. Клаузиус).
Невозможно при помощи неодушевлённого материального двигателя непрерывно получать работу, только охлаждая какую-либо массу вещества ниже температуры самой холодной части окружающей среды (В. Томсон)
Свободная и связанная энергия.
Из формулировки 2 зкона следует, что не весь запас внутр энергии системы при постоянной темературе может превращаться в работу-это физический смысл 2го закона
Условно, внутр энергию системы можно представить U=F+Q
F-свободня энергия(часть вн. Энергии,способная производить работу)
Q-связанная эрергия
Т.к U и F ф-ции состояния, то ∆U=∆F+Q
Толкование энтропии (S)-функция состояния, которая служит мерой беспорядка(неустойчивости) системы
Вычисление S в различных процессах
1.изотермический-т-пост
∆S=Q/T [S]=Дж/кк
2.неизотермич
∆S=C* lnT2/Т1 = 2,3С * lg T2/Т1
С-молярная теплоемкость в-в
∆S>0 процесс протекает самопроизв
Энтропия с точки зрения классической термодинамики (энтропия как мера связанной энергии). Определение энтропии, расчет энтропии веществ в различных процессах (изотермический, изобарный, изохорный), стандартная энтропия, расчет DS химической реакции. Свойства энтропии.
Энтропия- мера связанной энергии, т.е. количество связанной энергии, приходящейся на 1К.
Понятие энтропии было впервые введено в 1865г. Рудольфом Клаузиусом. Он определил изменение энтропии термодинамической системы при обратимом процессе как отношение общего количества тепла ΔQ к величине абсолютной температуры Т (т.е. тепло, переданное системе, при постоянной температуре).
· Изотермический процесс (Т=const):
ΔS= ΔQ/Т
[S] = Дж/К
· Неизотермические процессы ( изобарный (Р=const), изохорный (V=const)):
ΔS= С*lnT2/ Т 1 = 2,3*lg lnT2/ Т1 , где С-молярная теплоемкость в-ва.
Стандартная энтропия (S298) – абсолютное значение энтропии 1 моля в-ва, рассчитанное для стандартных условий.
[S298] = Дж/моль*К
ΔS298 =∑nS 298(прод.) - ∑nS 298(исх.)
Свойства энтропии:
1. Энтропия тела при абсолютном нуле равна нулю.
2. Энтропия веществ может быть только положительной величиной.
3. Энтропия является величиной аддитивной: энтропия сложной системы равна сумме энтропий ее частей.
Зависимость скорости реакции от концентрации реагирующих веществ (закон действующих масс). Константа скорости.
Закон действующих масс сформулирован в 1867 г. норвежскими учеными К. Гульдбергом и П. Вааге: скорость простой реакции в каждый момент времени пропорциональна произведению концентраций реагирующих веществ, возведенных в степени, равные коэффициентам в стехиометрическом уравнении.
-для гомогенной реакции:
аА + bB= fF + dD
Математическое выражение ЗДМ:
V= k* Cа А * Cb B ,где
k- константа скорости.
Примечания:
1.математическое выражение ЗДМ называется кинетическим уравнением.
2.сумма показателей степеней в кинетическом уравнении, как правило, не больше 3.
a+b≤ 3
3.ЗДМ применим только к гомогенным, простым реакциям или к отдельным стадиям сложных.
Если изменить концентрацию реагирующих в-в, скорость системы или давление, то скорость данной р-ции изменится в соответствии с ее кинетическим ур-нием.
Физический смысл константы скорости.
аА +bB= fF + dD
CА =CВ = 1моль/л
Са А * Сb B =1
В случае гомогенной р-ции, кинетическое ур-ние будет иметь вид V= k. Вывод: константа скорости хим. р-ции (при условии, что концентрация реагирующих или их произведение в соответствии со степенями) равна 1.
В случае гетерогенной р-ции, в кинетическое ур-ние входят только концентрации газообразных и жидких в-в. Концентрация твердого в-ва , на поверхности которого протекает р-ция , изменяется незначительно, считается величиной постоянной, не включается в ур-ние.
Зависимость скорости реакции от температуры. Правило Вант-Гоффа, особенности температурного коэффициента для биохимических процессов. Уравнение Аррениуса. Энергия активации.
В 1884 г. Вант-Гофф установил, что при повышении температуры на 10 градусов скорость многих реакций увеличивается в 2–4 раза.
Математически эта зависимость выражается соотношением:
Vt2 = Vt1*ɣ^t2-t1/10,
Kt2= kt1*ɣ^t2-t1/10
где V2 и V1 — скорости реакции при температурах t1 и t2,
k - константа скорости,
ɣ — температурный коэффициент скорости реакции.
Для многих реакций ɣ имеет значения в пределах 2–4.
Если t2-t1=10, то Vt2/Vt1= k t2/k t1= ɣ или что одно и тоже ɣ=Vt+10/Vt=kt+10/kt
Физический смысл температурного коэффициента.
Из последнего ур-ния следует, что ɣ- величина, показывающая во сколько раз увеличивается скорость р-ции или константа скорости при увеличении температуры реакционной смеси на 10 градусов.
Ферментативные р-ции имеют более высокие значения температурного коэф.
ɣ= 7-10 (процессы денатурации белка)
Все жизненные процессы протекают в небольшом температурном интервале.
Уравнение Аррениуса.
k=A* e^-Ea /R*T, где
k- константа скорости,
А- постоянная для данной р-ции величина= общему числу соударения в единицу скорости за единицу времени,
е- основание натурального логарифма,
Еa- энергия активации- количество энергии, которое необходимо сообщить молекулам реагирующих в-в, чтобы они при столкновении могли вступить в хим.взаимодействие,т.е. стали активными,
R- универсальная газовая постоянная,
Т- абсолютная температ. процесса.
КБС.
· При добавлении сильной кислоты в реакцию вступает солевой компонент и наоборот.
Пр.: ацетатная БС.
CH3COONa + HCl= CH3COOH + NaCl
CН3COO- + H+= CH3COOH
При добавлении сильной кислоты образуется эквивалентное кол-во слабой уксусной кислоты, являющейся компонентом БС. Увеличение концентрации CH3COOH, в соответствии с законом разведения Освальда, приводит к уменьшению степени ее диссоциации. В результате этого концентрация Н увеличивается незначительно и рН практически не меняется.
· При добавлении щелочи.
CH3COOH + NaOH= CH3COONa + H2O
CH3COOH + OH- =CH3COO - + H2O
Гидроксид-ионы, влияющие на реакцию среды, превращаются в эквивалентное количество воды, являющейся слабым электролитом. Уменьшение концентрации CH3COOH увеличивает ее степень диссоциации, следовательно, увеличения рН из-за расходования уксусной кислоты не происходит.
ОБС.
· При добавлении сильной кислоты в реакцию вступает основный компонент, а при добавлении щелочи- солевой.
Пр.: аммиачная БС.
NH4ОН + HCl= NH4Cl + H2O
NH4OH + H+=NH4+ + H2O
Механизм действия ОБС при добавлении сильной кислоты аналогичен мех-му действия КБС при взаимодействии со щелочью
· При добавлении щелочи.
NH4Cl + NaOH= NH4ОН+ NaCl
NH4++ ОН - = NH4ОН
Механизм действия ОБС при добавлении щелочи аналогичен мех-му действия КБС при добавлении сильной кислоты.
Амфолитные БС
При взаимодействии АБС с кислотой в реакцию вступает концентрированная кислотная группа (акцептор Н+), а при взаимодействии со щелочью- концентрированная основная группа(донор Н+). В результате ионы, влияющие на реакцию среды, нейтрализуются и рН практически не меняется.
Пр.: белковая БС.
· Взаимодействие с сильной к-той.
· Взаимодействие со щелочью
В процессе нейтрализации белковые частицы приобретают заряд: при взаимодействии с к-той- положительный, при добавлении щелочт- отрицательный.
Разбавление водой.
Разбавление БР в 10,20 и более раз незначительно влияет на их рН.
Из уравнения Г-Г видно, что при разбавлении БР, концентрации компонентов уменьшаются одинаково, и их отношение не меняется, следовательно, не меняется рН
Механизм действия.
При накоплении в организме кислых продуктов они вступают в реакцию нейтрализации с бикарбонатом Na с образованием NaCl и H2CO3 (который диссоциирует на CO2 и H2O) CO2 с помощью гемоглобиновой буферной системы переносится в легкие, а оттуда выводится из организма. Таким образом существует связь между этими двумя буферными системами.
NaHCO3 + НCl NaCl + H2CO3 (диссоциирует на)
H2O CO2
При появлении в крови избытка щелочных продуктов в реакцию вступает второй компонент буферной системы H2CO3, в результате чего образуется бикарбонат Na и вода. Избыток NaHCO3 удаляется через почки.
H2CO3 + NaOH NaHCO3 + H2O
Таким образом, благодаря легким и почкам соотношение между NaHCO3 и H2CO3 поддерживается на постоянном уровне равном 20:1 (это соотношение свидетельствует о том, что щелочной компонент буфера должен быть больше кислотного резерва т.к. вероятность образования в организме кислого продукта намного выше).
Фосфатная буферная система.
1% от всей емкости крови. Она представлена солями фосфорной кислоты: двух и одного замещенного фосфорнокислого Na.
Na2HPO4/ NaH2PO4 = 4:1
Механизм действия.
При появлении в среде кислого продукта появляется однозамещенный NaH2PO4-менее кислый продукт, а при защелачивании двузамещенный Na2HPO4.
Действие фосфатного буфера связано с действием почек, а механизм регуляции, как и у бикарбонатной буферной системы, т.е. при закислении среды в почках возрастает секреция ионов водорода в просвет канальцев, где эти ионы вступают в реакцию с двузамещенным фосфорнокислым Na (Na2HPO4) и образованием Na2H2PO4 который выделяется с мочой, и наоборот.
HPO42- + H+ H2PO4-
H2PO4- + OH- HPO42- + H2O
Белковая буферная система.
Имеет меньшее значение для поддержания К.О.С. в плазме крови.
Механизм :
1. Взаимодействие с кислотой
(NH4)+-R-(COO-)+H+=(NH3)+ -R-(COOH)
2. Взаимодействие со щелочью
(NH3)+ -R-(COO-)+ OH- =(NH2) -R-(COO-)+H2O
Коррекция КОС
Ацидоз- вводят гидрокарбонат Na
Протекающие процессы
1. Диссоциации NaHCO3
NaHCO3 = Na+ +HCO3-
2. Нейтрализация избытка H+
H++ HCO3- = H 2CO3 В рез-те образуется слабая кислота
Алкалоз- вводят внутривенно кислотный р-р глюкозы, получаемый добавление 100мл 1% р-р HCL к 1л 5% р-ра глюкозы
Протекающие процессы
1. Диссоциация сильной кислоты
HCL= H+ + CL-
2. Нейтрализация OH-
H++ OH- = H 2O
В результате ион, влияющие на реакцию среды нейтрализуются, превращаясь в слабый электролит воду
Классификация
1) По заряду: кислые, анионные(электролиты), нейтральные (неэлектролиты)
K4[Fe(CN)6]- анионное
2) По природе лигандов:
- Аквакомплексы (L- H2O)
- Амминокомплексы (L- NH3)
- Гидрокомплексы (L- ОН-)
- Ацидокомплексы (L- анионы кислот)
- Смешенные лигандные комплексы (различные L)
- Внутрикомплексные соединения (хеланты)
Ст.
[Ag(NH3)2]+ = [Ag(NH3)]+ NH3
Вторичная диссоциация
Ст.
[Ag(NH3)]+ = Аg+ + NH3
Сложив левую и правую части, получим сумму диссоциаций
[Ag(NH3)2]+ = Аg+ + 2NH3
Применив закон действующих масс для постоянного химического равновесия получим:
Кн= [Ag+]*([NH3]-)2/[[Ag(NH3)2]+], где Кн- константа нестойкости Кн=Кд(Кк)=Кравновесия
Кн является мерой устойчивости комплексной частицы. Чем больше устойчивость, тем меньше образуется простых частиц при диссоциации, тем меньше Кн.
Величина обратная Кн- константа устойчивости Ку.
Ку=1/Кн
Чем прочнее комплекс, тем больше Ку
ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ Кн И Ку.
С их помощью можно предсказать возможность протекания реакций с участием КС
Реакция возможна, если Кн<Кн(исх. компл.). Образование более устойчивое
Комплексное соединение.
Кн связано с ∆G реакции диссоциации комплекса уравнением изотермы химической реакции
| ∆G=-RTLnКн=2,3RTLgКн |
28. Металлоферменты и другие биокомплексные соединения: гемоглобин и его производные, цитохромы, каталаза, пероксидаза, витамин В12 (пространственное строение, функции, электронное строение и тип гибридизации комплексообразователя)
Гемоглобин состоит из глобина (высокомолекулярный белок). Состоит из 4 субъединиц (2 α и 2 β) К каждой спирали присоединён гемоглобин.
Гемоглобин КС железа (+2) с протопорфином(ароматический, небензоидный, плоский, макроциклический, состоящий из 4 гетероциклов, 5 членное соединение с 1 атомом N.
Соединения между гетероциклическими метиленовыми группами. Метиленовые группы не принимают участие в связи с Fe.
ПРОТОПОРФЕРИНОВОЕ КОЛЬЦО
Простое строение определяется типом гибридизации комплексообразователя Fe+2d2sp3 КЧ
Октаэдр
| Ст.ок. | H | H-C | Символ, формула |
| +2 | H2O | Гемоглобин (дезоксигемоглобин) | HHb |
| +2 | O2 | Оксигемоглобин | HHbO2*(В пр.дых) |
| +2 | CO | Карбоксигемоглобин | HHbCO(в пр.дых) |
| +2 | CO2 | Карбоксигемоглобин | HHbCO2*( в пр.дых) |
| +3 | OH- | Метгемоглобин не прис-т O2 не уч-т в пр.дых-я | HHbOH- |
Каталаза, пероксидаза, цитохром С (ЦТХЗ) витамин B12(формула витамина!!!)
Является металоферментом
ЦТХС(формула в интерн.)
Основное отличие от гемоглобина- отсутствие переменного лиганда, то есть все лиганды(L) постоянны.
ЦТХС является католизатором различных реакций. Участвует в переносе энергии в митохондрии. Перенос энергии осуществляется благодаря реакции.
Физические
А. метод замены растворителя– получается из истинного раствора путем добавления растворителя.
Условия получения:
1.объем истинного раствора намного больше объема нового растворителя.
2.ДФ плохо растворяется в новом растворителе.
3.оба растворителя хорошо смешиваются друг с другом.
Пример: при добавлении 5 мл воды несколько капель спиртового раствора канифоли образуется коллоидный раствор, что можно установить появлением голубого окрашивания.
2.Химический – они основываются на химических реакциях, в результате которого образуются нерастворимые в воде вещества. Для получения золей химическим методом необходимо два условия:
1 – это невысокая концентрация исходных растворов
2 – избирательность одного из реактивов
Метод окисления.
2H2S + O2 = HS + H2O
S-2-2 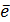 = S0 восстановитель, окисление
= S0 восстановитель, окисление
O20 +4 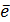 = 2O-2, окислитель, восстановление.
= 2O-2, окислитель, восстановление.
Метод восстановления – реакция присоединения электрона ионами, которые затем превращаются в атомы, конденсируются в качестве каллоидной частицы.
В качестве восстановителя используется водород, формалин, танин.
Ag2O + H2 = 2Ag + H2O
Метод гидролиза – при получении изолей из солей, в результате реакции образуются плохо растворимые вещества.
FeCl3 + 3 H2O = Fe(OH)3 + 3HCl
Fe(OH)3 + HCl = FeOCl + 2 H2O
FeOCl = Feo+ + Cl-
Метод обменного разложения – основан на взаимодействии двух веществ. В результате реакции образуется новое труднорастворимое вещество, способное сохраняться в высоко дисперсном состоянии
2H3AsO3 + 3H2S = As3S2 + 6H2O
{[mS]nHS-(n-x)H+}x-xH+
Понятие биогенности химических элементов: химические элементы в организме человека, их классификация по степени важности для процессов жизнедеятельности, биогенные элементы в периодической системе. Биосфера, круговорот биогенных элементов в природе. Кларки элементов.
Биогенными называются элементы, необходимые для построения и жизнедеятельности различных клеток и организмов.
БЭ в периодической системе:
I Н
II все кроме Be,Ne
III все кроме Ar
IV все кроме Se,Ga,Ge,Kr
V Sr,Mo,Cd, Sn,I
Примечания: 1. Всего в ПС 33 БЭ: 7 s-элементов, 11 d-элементов, 15 р- элементов
2.большинство БЭ находятся в II-IV
3. Среди БЭ нет инертных газов
Классификация БЭ по степени значимости для жизнедеятельности (В.В.Ковальский):
1.Жизненно необходимые (незаменимые) элементы. Они постоянно содержатся в организме человека, входят в состав ферментов, гормонов и витаминов: Н,О,Са,N,K,P,Na,S,Mg,Cl,C,I,Mn,Cu,Co,Fe,Zn,Mo,V.
2.Примесные элементы. Эти элементы постоянно содержатся в организме животных и человека, но их биологическая роль мало выяснена: Ga,Sb,Sr,Br,F,B,Be,Li,Si,Sn,Cs,Al,Ba,Ge,As,Rb,Pb,Ra,Bi,Cd,Cr,Ni,Ti,Ag,Th,Hg,U,Se.
3.Примесные элементы обнаружены в организме человека и животных, но данные о количестве и их биологическая роль не выяснены: Sc,Tl,In,La,Pr,Sm,W,Re,Tb
Биосфера- часть земной оболочки, занятая растительными и животными организмами. По Вернадскому, биосфера- это определенным образом организованная среда, переработанная живыми организмами и космическими излучениями и приспособленная к жизни.
Распространенность (кларки) хим.элементов в земной коре различна. Около 50% массы земной коры приходится на кислород, более 25%- на кремний. Восемнадцать элементов- кислород, кремний, алюминий, железо,кальций,натрий,калий,магний,водород,титан,углерод,хлор,фосфор,сера,азот,марганец,фтор,барий- составляют 99,8% массы земной коры. На долю всех остальных элементов приходится лишь 0,2%.
Согласно Вернадскому, живые организмы принимают активное участие в перераспределении хим. элементов в земной коре. Особое значение имеют круговороты биогенных хим.элементов, прежде всего углерода. Растительные организмы извлекают из атмосферы до 300 млрд. т углекислого газа ежегодно. Растения частично поедаются животными, частично отмирают. Орг. вещество в результате дыхания организмов, разложения их остатков, процессов брожения и гниения превращаюся в углекислый газ или отлагается в виде гумуса, торфа.
Железо (Fe)
В организме содержится 5-5,5 г, большая его часть 70-80% находится в гемоглобине.
Ежедневная доза- 1,2 мг. Ежедневное потребление 10-20 (5-10) мг
Из пищи поступает в организм только 10-20% железа.
Недостаток Fe вызывает железодефицитную анемию. Соединения железа выполняют каталитическую, транспортную, буферную функцию.
Цинк (Zn)
В организме содержится 2,3 г.
Суточная потребность 13 мг.
Биологическая роль Zn обусловлена постоянным зарядом его иона. Известно более 40 металлоферментов , активирующих гидролиз белка, пептидов.
Zn влияет на основные процессы кроветворения, размножения, роста и развития организма.
Медь (Cu)
В организме содержится 100 мг.
Суточная норма- 2-3 мг
Главная функция- ферментативная. Известно около 25 медьсодержащих ферментов. Участие меди в ОВР основано на легкости превращения: Cu2+ +e=Cu+
Cu участвует в кроветворении
Марганец (Mn)
В организме содержится 12 мг.
Суточная потребность 5-7 мг.
Присутствует в виде ионов M2+ или в комплексе с белками, амк.
Функция- регуляция активности различных ферментов. Активируя АТФ, марганец участвует в процессах аккумуляции и переноса энергии. Мn стабилизирует структуру нуклеиновых кислот.
Молибден (Мо)
В организме содержится 9 мг.
С пищей потреб. 0,2-0,3 мг/сут.
Входит в состав ферментов, которые катализируют окислительно- восстановительные процессы. Входе этих реакций, его степень окисления с +6 уменьшается до +5,+4, происходит восстановление. При избыточном поступлении молибдена происходит активация синтеза ксантиноксидазы.
Хром (Cr)
Содержание в организме 6-6,6 мг
Суточная потребность- 0,15мг.
Преимущественно концентрируется в костях, содержится в эритроцитах.
Cr участвует в обмене НК, входит в состав ферментных систем. Иона Cr3+ участвуют в стабилизации НК.
Кобальт (Со)
В организме содержится 1,2 мг.
Ежедневное потребление- 0,3 мг.
5-10% входит в состав витамина В12, Со единственный из металлов, входящий в структуру витамина. Участвует в ОВР организма, поскольку возможен процесс:
Со3+ +е= Со2+
Со влияет на минеральный, липидный обмен, участвует в кроветворении. Недостаток Со вызывает злокачественную анемию.
Номенклатура органиеских соединений.Понятие о структурной изомерии органических соединений . Строение атома углерода , типы гибридизации и виды ковалентной связи в орг соединениях. Связь пространственного строения орг. соединений с их биолог активностью
Названия углеводородов и алкильных групп:
| Метан | СН4 | Метил | СН3- |
| Этан | С2Н6 | Этил | С2Н5- |
| Пропан | СН3СН2СН3 | Пропил Изопропил | СН3СН2СН2- СН3СНСН3 |
| Бутан | СН3СН2СН2СН3 | Бутил Изобутил Втор. бутил Трет. бутил | 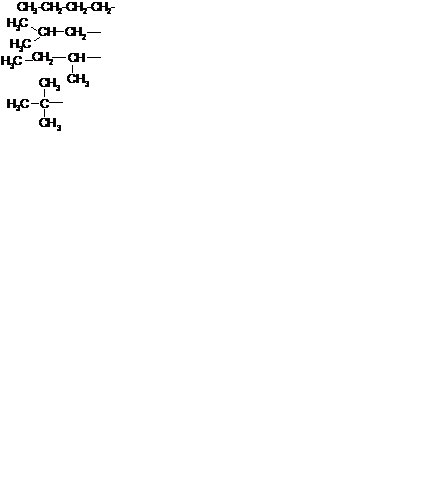
|
по номенклатуреIUPAC
( заместительная номенклатура)
Для составления названия органического соединения по номенклатуре IUPAC необходимо выполнить следующие операции:
1. Определите функциональную (характеристическую) группу, если она имеется, суффикс которой используют при составлении названия. При составлении названия используется суффикс только одной функциональной группы, называемой главной ( исключение: суффиксы двойной или тройной связи). Все заместители, в том числе и другие младшие функциональные группы, указываются префиксами.
Некоторые характеристические группы, расположенные
в порядке уменьшения старшинства
| КЛАСС | Формула | ПРЕФИКСЫ | СУФФИКСЫ |
| Карб.к-ты Альдегиды Кетоны Спирты Фенолы Амины | -СООН -(С)ООН -СНО -(С)НО -(С)=О -ОН -ОН -NH2 | -карбокси - -формил -оксо -оксо -гидрокси -гидрокси -амино | -карб. кислота -овая кислота -карбальдегид -аль -он -ол -ол -амин |
2. Определите родовой гидрид:
а) для ациклических соединений родовым гидридом является самая длинная неразветвленная цепь, включающую главную функциональную группу а также двойные и (или) тройные связи. Родовой гидрид образуется прибавлением атомов водорода вместо заместителей или гетероатомов, присоединеннных к длинной цепи, чтобы получился насыщенный углеводород.
б) для циклических соединений родовым гидридом является насыщенный циклоалкан, например циклогексан или полностью ненасыщенный углеводород ( гетероциклическое соединение), например бензол, пиридин и т.д.
3. Назовите родовой гидрид вместе с суффиксом главной группы.
4. Пронумеруйте самую длинную цепь таким образом, чтобы атом углерода главной функциональной группы получил наименьший номер.
5. Назовите заместители вместе с цифрами(локантами), указывающими атомы углерода, при которых заместители находятся и присоедините их к названию родового гидрида. Локанты двойной и (или) тройной связи и локант главной функциональной группы расположите перед соответствующими суффиксами.
1-ый пример
Н3С - СН2 - ОН НО - СН2 - СН2 - ОН
Главная группа: -ОН -ол
Родовой гидрид: Н3С - СН3 этан
Название: этанолэтандиол-1,2
2-ой пример:

3-ий пример:


Пространственные изомеры: Энантиомеры

Строение атома углерода
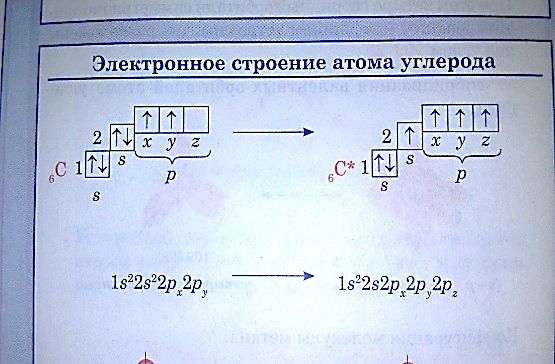
Типы гибридизации
В зависимости от числа вступивших в гибридизациб орбиталей том углерода может находиться в 3 видах гибрид-ии
1.первое валентное состояние sp3 гибр- при комбинации 1 s и 3 p орбиталей,
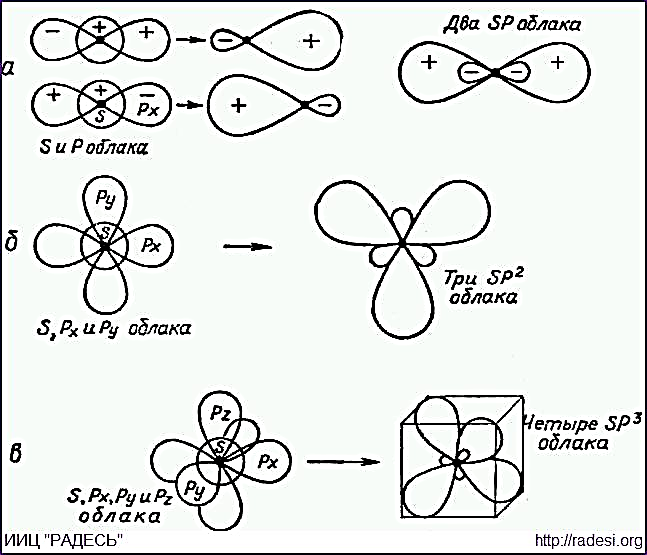
2. Sp2- 1s и 2p
3. Sp -1s и 1p
Ковалентная связь-хим связь, образованная за счете обобщения электронов связываемых атомов-осн тип связи в орг в-вах
Неполярная КС-связь, образованная между атомами с одинаковой электроотрицательностью, при которой связующее электронное облако равномерно распределено в обасти пространства между ядрами данных атомов
Полярная КС- связь, образованная между атомами с разной электроотрицательностью, при которой связующее электронное облако смещено в сторону более электроотрицательного атома
КС бывают 2х типов: сигма и пи связи
Сигма связь-связь,образованная при осевом перекрывании атомной орбиталей с расположением максимума перекрывания на прямой ,соединяющей ядра связываемых атомов
Пи связь-образована при бороков перекрывании p-АО
46-Реакция электрофильного присоединения: гетеролитическая реакция с участием π-связи между sp2-гибридизованными атомами углерода (галогенирование, гидрогалогенирование, гидратация).
АЕ- реакция электрофильного присоединения.
Ненасыщенные углеводороды – алкены, циклоалкены, алкадиены и алкины проявляют способность к реакциям присоединения, так как содержат двойные или тройные связи. За счёт π-электронов в молекулах таких соединений имеется довольно обширная область отрицательного заряда. Поэтому они представляют собой нуклеофилы и, следовательно, склонны подвергаться атаке электрофильной частицей (электрофильмым реагентом).
Галогенирование.
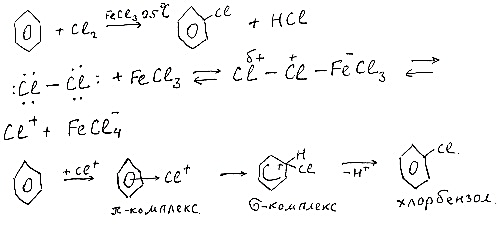
Нитрование.
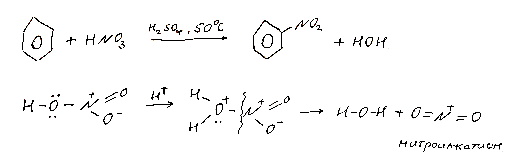
Алкинирование.
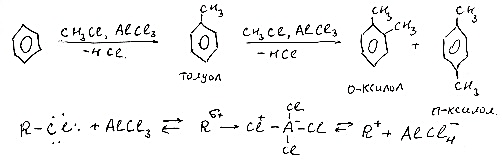
48-Реакция нуклеофильного замещения у sp3-гибридизованного атома углерода: гетеролитические реакции обусловленные поляризацией ϭ-связи углерод-гетероатом (галогенпроизводные, спирты).
SN-Реакция нуклеофильного замещения
SN наиболее характерны для насыщенных органических соединений, содержащих следующие функциональные группы: галоген, гидроксильную, тиольную и аминогруппу.
SN1 – характерны характерны для третичных и частично вторичных алкангалогенидов при наличии слабого нуклеофила и полярного растворителя
Механизм:
I стадия
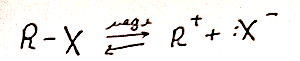
II стадия
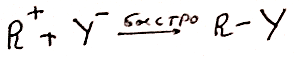
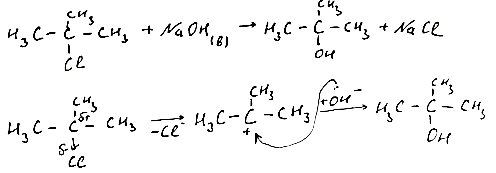
SN2-характерен для первичных и частично вторичных атомомв.
Механизм:
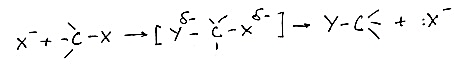
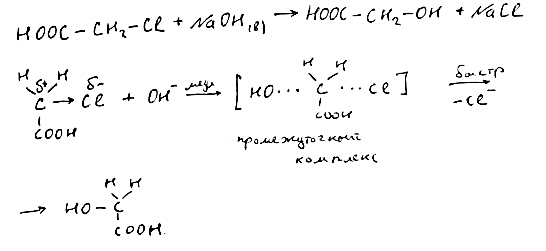
49-Реакция нуклеофильного присоединения: гетеролитическая реакция с участием π-связи углерод-кислород (взаимодействие альдегидов и кетонов со спиртами, первичными аминами). Влияние электронных и пространственных факторов, роль кислотного катализа. Биологическое значение реакции нуклеофильного присоединения.
AN-Реакция нуклеофильного присоединения.
Характерны для альдегидов и кетонов.
Большое значение в биологическом плане имеет реакция карбонильных соединений (альдегидов и кетонов) с аммиаком, при этом образуются имины (основания Шиффа), очень неустойчивые, легкогидролизующиеся соединения.
Имины являются промежуточными продуктами в некотоорых ферментативных реакциях, при синтезе аминов из альдегидов и кетонов.
Например, в организме по такой схеме синтезируются некоторые α-аминокислоты.
Взаимодействие аммиака с альдегидами может осложняться возможной циклизацией. Так, из формальдегида А.М. Бутлеров впервые получил медицинский препарат – гексаметилентетраамин (уротропин), получивший широкое применение в качестве антисептического средства.
Кислотный катализ служит для активации субстрата.
Реакционные центры.
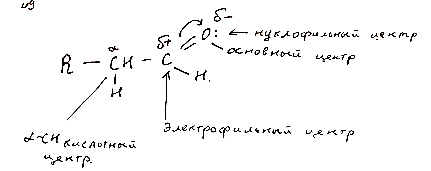
Механизм:
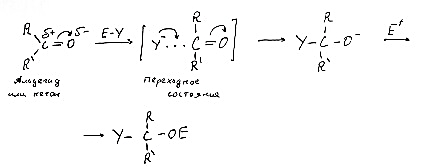
В реакцияхAN для увеличения скорости реакции используется катализатор (неорганическая кислота)
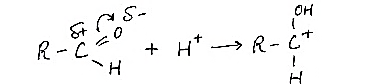
Схема:
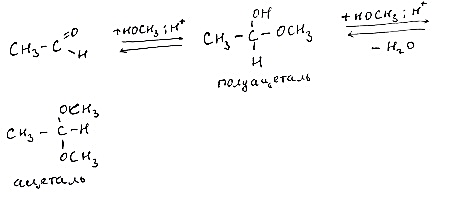
Механизм:
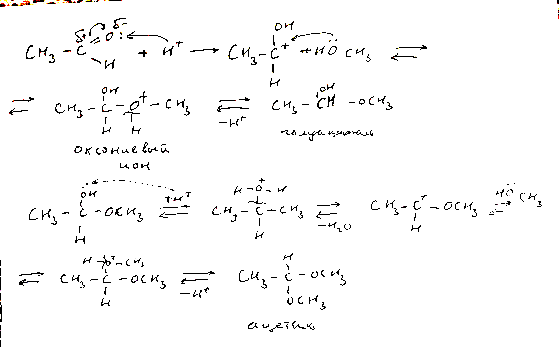
Высшие жирные кислоты (ВЖК)
В состав омыляемых липидов входят различные карбоновые кислоты от С4 до С28. Это в основном монокарбоновые кислоты с неразветвленной цепью и четным числом атомов углерода, что определяется особенностями биосинтеза. Наиболее распространены кислоты с числом атомов углерода 16-18.
CH3(CH2)14COOHС15Н31СООН пальмитиновая кислота
CH3(CH2)16COOHС17Н35СООН стеариновая кислота- входит в виде глицеридов в состав липидов, прежде всего триглицеридов жиров животного происхождения, последние выполняют функцию энергетического депо.
CH3(CH2)7СН = СН(CH2)7СООН С17Н33СООН олеиновая кислота
CH3(CH2)4СН = СНСН2СН = СН(CH2)7СООН С17Н31СООН линолевая кислота
CH3CH2СН = СНСН2СН = СНСН2СН = СН(CH2)7СООН С17Н29СООН линоленовая кислота
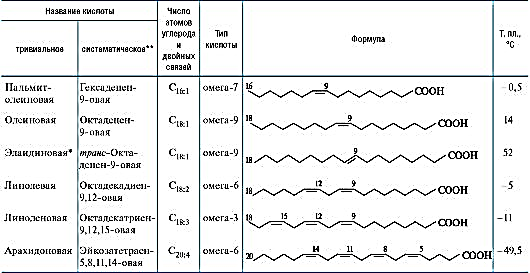
CH3(СH2)4СН = СНСН2СН = СНСН2СН = СНСН2СН = СН(CH2)3СООН С19Н31СООН арахидоновая кислота
Собственная номенкатура ненавыщенных ВЖК: концевой атом угерода обозначается ϖ(омега) отсчет двойных связей производится не как обычно от карбоксильной группы, а от метильной группы.
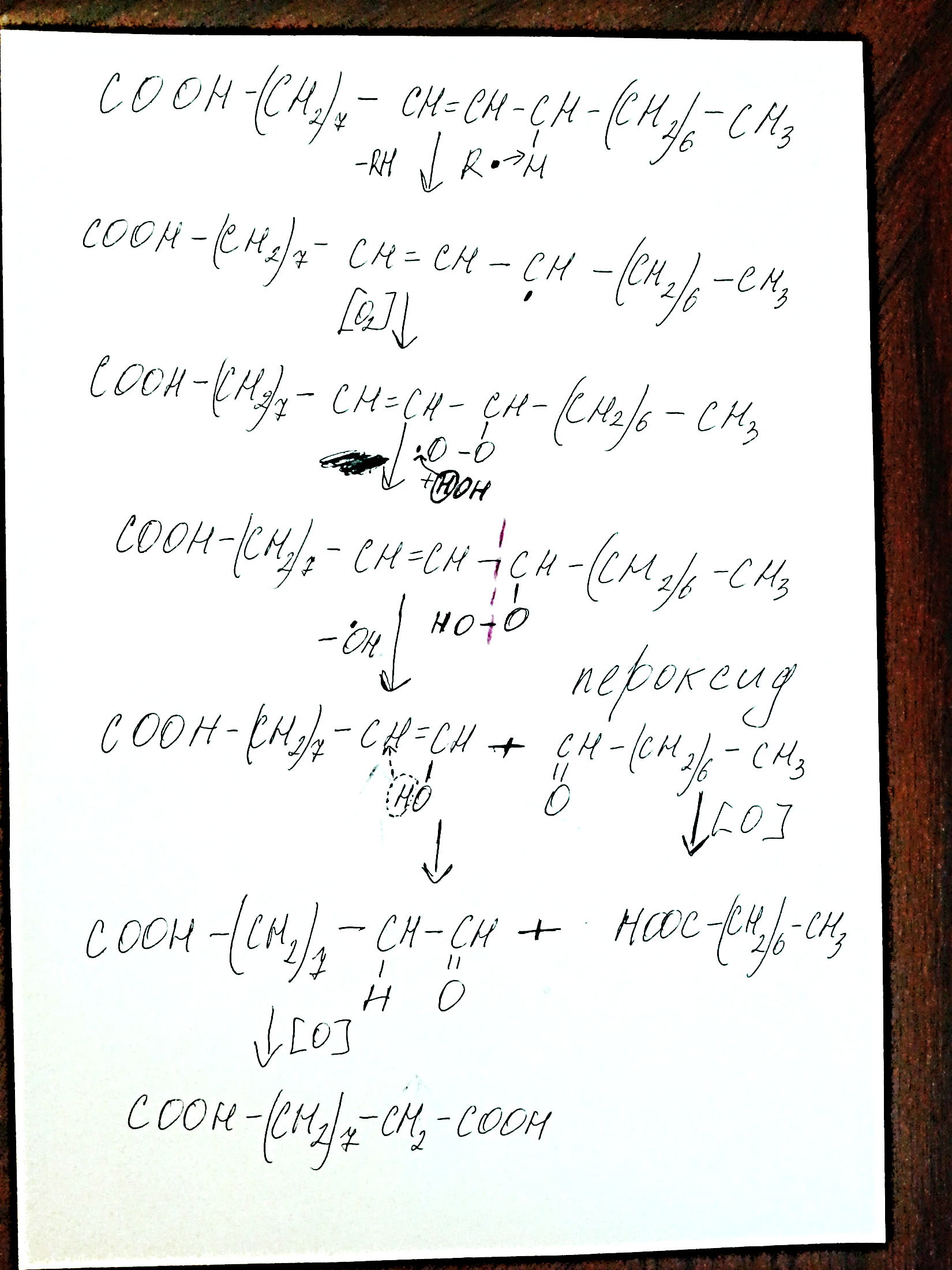
63.Перикисное окисление липидов.
ЦИКЛО-ОКСО-ТАУТОМЕРИЯ
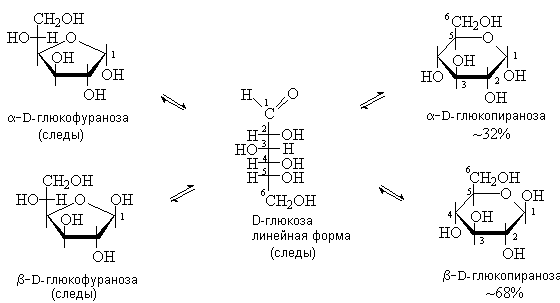
Циклические формы моносахаридов изображают с помощью формул Хеуорса. Молекулу представляют в виде плоского цикла, перпендикулярного плоскости рисунка.
Циклические, особенно пиранозные формы, энергетически более выгодны для большинства моносахаридов. Например, в растворе D-глюкозы преобладает b-D-глюкопираноза
Существование равновесия между линейной и циклическими формами моносахаридов получило названиецикло-оксо-таутомерии.
66.Дисахариды: стрение, типы гликозидной связи, образование, гидролиз, цикло-оксо-таутомерия. Востанавливающие(мальтоза, лактоза, целлобиоза), невостанавливающие(сахароза), дисахариды.
