Для практики представляют интерес однокомпонентные двухфазные системы. Такие системы образуются при следующих превращениях:
плавление испарение
Т 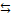 Ж Ж
Ж Ж 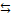 П
П
кристаллизация конденсация
полиморфные сублимация
Тα 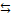 Тβ Т
Тβ Т 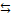 П
П
превращения конденсация
Для таких систем применяется уравнение Клапейрона, которое характеризует зависимость температуры фазового перехода от внешнего давления.
Применим уравнение Клапейрона к равновесию между 2 конденсированными фазами (Тв → Ж)
dT/dP Тпл. (Vж -Vт )/∆Hпл.
Тпл. - температура плавления
∆Н пл. - изменение энтальпии при плавлении
Т.к. процесс плавления вещества - эндотермический (ΔН>О), то знак dT/dP определяется только разностью объемов жидкой и твердой фаз. Если Vж-Vт>О, то dT/dP>О. Следовательно, когда плавление вещества сопровождается увеличением V, с повышением внешнего давления температура плавления вещества увеличивается. Такая закономерность характерна для большинства веществ.
Если Vж-Vт<О, то dT/dP<О. Следовательно, когда плавление вещества происходит с уменьшением объема системы, с повышением внешнего давления температура плавления вещества уменьшается. Такая закономерность справедлива для меньшего числа веществ, например, для воды, галлия, висмута, некоторых сортов чугуна.
Для равновесия жидкость-пар уравнение Клапейрона принимает вид:
dT/dP = Tk.(Vп.-Vж.)/ΔНк.,
где Тк. - температура кипения; ΔНк.- изменение энтальпии при испарении.
Так как ΔНк.>О и Vп.> Vж., с повышением внешнего давления температура кипения жидкости всегда увеличивается.
Для расчетов производной dT/dP по уравнению необходимо знать молярные объемы веществ, а они часто не известны. Поэтому Клаузиус видоизменил уравнение для процессов испарения, конденсации и возгонки.
При температурах далеких от критической, объем парообразной фазы во много раз больше объема жидкой фазы. Если насыщенный пар подчиняется уравнению состояния идеальных газов, то Vп.- Vж.= RT/p, a
dP/dT =ΔНкP/RTк2 (а) или dlnP/dT=ΔHK./RTk2(б)
Эти уравнения называются уравнениями Клапейрона-Клаузиуса, они выражают зависимость давления насыщенного пара конденсированного вещества, равновесного с жидкостью, от температуры.
При интегрировании уравнения (б) получаем
lg Р2/р1 =ΔНфn /2,3R(1/T1-1/T2)=ΔНфn (Т2 –Т1 )/2,3RT2* T1
ДИАГРАММЫ СОСТОЯНИЯ ОДНОКОМПОНЕНТНЫХ СИСТЕМ
Для описания одно- и многокомпонентных систем Н.С.Курнаковым был предложен графический метод физико-химического анализа. Графическое изображение зависимостей р от Т (или р от С, Т от С) называется диаграммой состояния . Анализ диаграмм состояния позволяет определить число фаз, границы их существования, характер взаимодействия компонентов, наличие вновь образующихся соединений и их состав. Диаграммы позволяют проводить анализ без выделения индивидуальных компонентов.
Правило фаз для однокомпонентных систем принимает вид
С=1-Ф+2=3-Ф
Т.к. число степеней свободы не может быть отрицательным, следовательно, число фаз, находящихся в равновесии, не может быть > 3. По числу фаз может быть 3 типа однокомпонентных систем: одно-, двух-, трехфазные.
ДИАГРАММА СОСТОЯНИЯ ВОДЫ

(рис.1)
Состояние воды изучено в широком интервале температур и давлений. При высоких давлениях установлено семь кристаллических модификаций вещества - явление полиморфизма, которое приводит к усложнению диаграммы состояния.
Рассмотрим проекцию объемной диаграммы состояния воды на плоскость Р-Т при невысоких давлениях. На диаграмме имеются 3 поля: льда, жидкости и пара. В пределах каждого поля можно произвольно менять температуру и давление без изменения числа фаз, т.к. при Ф = 1
С= 1 - 1+2 = 2
Кривые ОС, ОВ, ОА характеризуют те значения Р и Т, при которых в системе имеются в" равновесии две фазы. Каждая из кривых показывает зависимость температуры фазового перехода от внешнего давления. Наклон кривых определяют по уравнению Клапейрона:
(dP/dT) ж 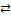 п =ΔН/T(Vп - Vж)
п =ΔН/T(Vп - Vж)
Т.к. Vп > Vж , то ΔV>0. Теплота испарения ΔΗ>0, поэтому при росте температуры, давление увеличивается и кривая ОВ наклонена вправо.
Линия ОА показывает зависимость температуры замерзания воды от внешнего давления. Применим уравнение Клапейрона:
(dP/dT) т 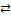 ж =ΔH/T(Vж - Vт )
ж =ΔH/T(Vж - Vт )
Для воды Vt>Vж , поэтому ΔV<0, то ( dP/dT) т 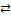 ж < О, и линия ОА наклонена влево.
ж < О, и линия ОА наклонена влево.
Система, заданная точкой на любой кривой моновариантна, т.е. имеет одну степень свободы С=3-2=1. Следовательно, произвольно можно изменять или давление, или температуру.
Точка О на диаграмме соответствует системе, в которой существуют три фазы (т. ж, п). В этом случае С=0 (система нонвариантна или инвариантна). В таком состоянии система может находиться при t= 0,01° С и давлении 1,033 х 105 Па.
На диаграмме имеется кривая ОД, которая является продолжением кривой ОВ, характеризующей равновесие ж 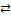 п. Кривая ОД соответствует равновесию.
п. Кривая ОД соответствует равновесию.
