По строению углеводородного радикалаα-аминокислоты делят на 7 групп:
I. Моноаминомонокарбоновые α-аминокислоты (нейтральные)
| H2N ¾ CH2 ¾ COOH |
Глицин (ГЛИ)
A-Аминоуксусная кислота
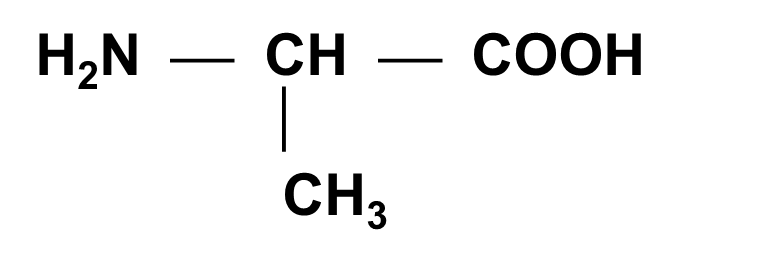
Аланин (АЛА)
A-Аминопропионовая кислота
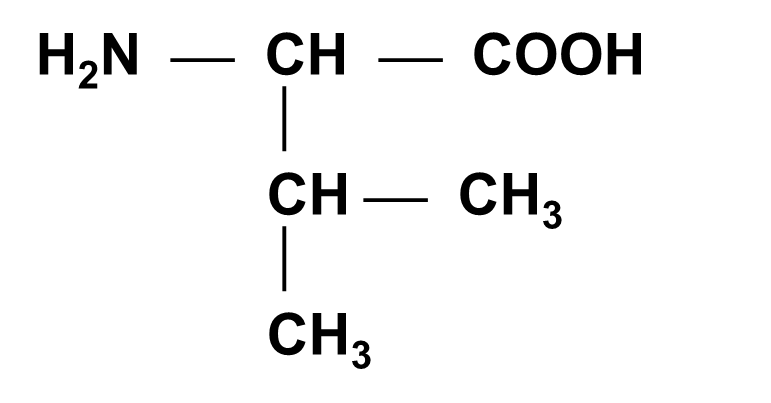
Валин (ВАЛ)
A-Амино-b-метилмасляная кислота
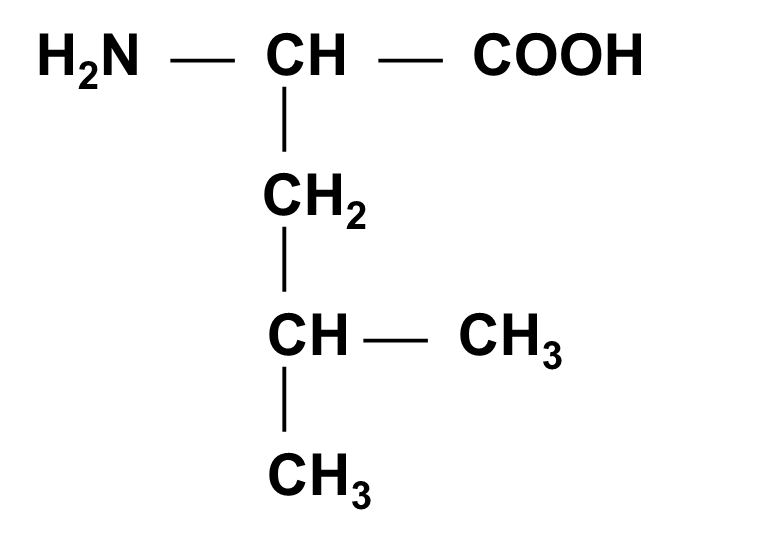
Лейцин (ЛЕЙ)
A-Амино-g-метилвалериановая кислота
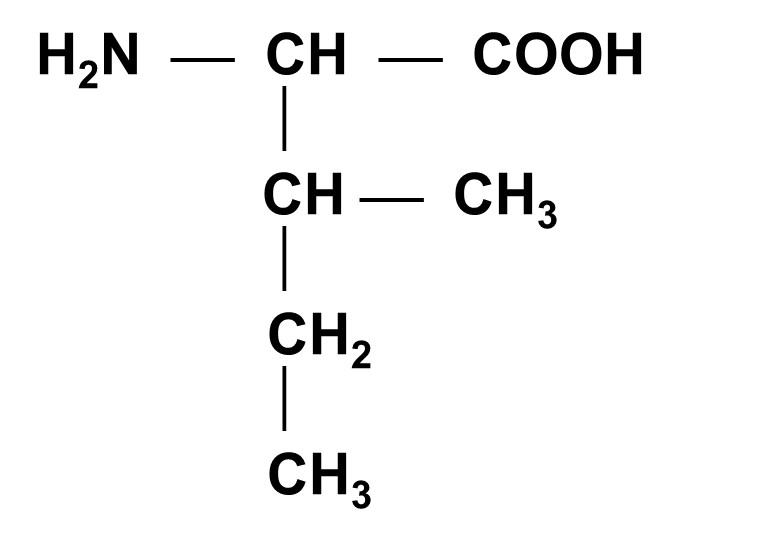
Изолейцин ( ИЛЕ )
A-Амино-b-метилвалериановая кислота
Боковые радикалы a-аминокислот этой подгруппы гидрофобные.
II. Моноаминодикарбоновые α-аминокислоты (кислые)
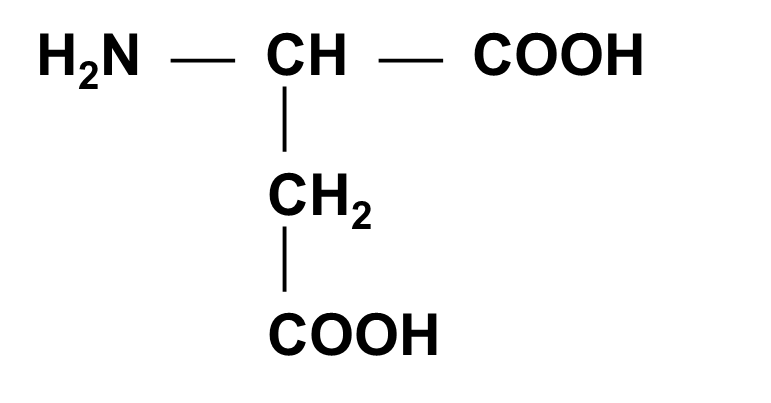
Аспарагиновая кислота (АСП)
A-Аминоянтарная кислота
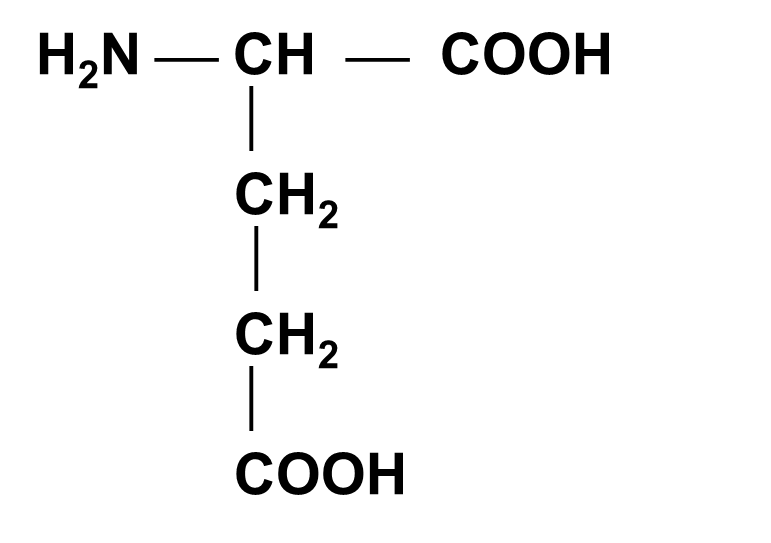
Глутаминовая кислота (ГЛУ)
A-Аминоглутаровая кислота
Боковые радикалы a-аминокислот этой подгруппы гидрофильные, ионогенные, несут отрицательный заряд (-OOC ¾ CH2 ¾ ).
В состав белков входят амиды данных кислот.
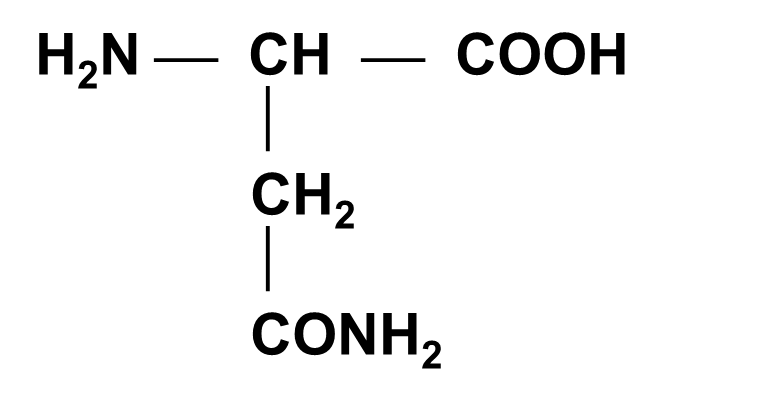
Аспарагин (АСН)
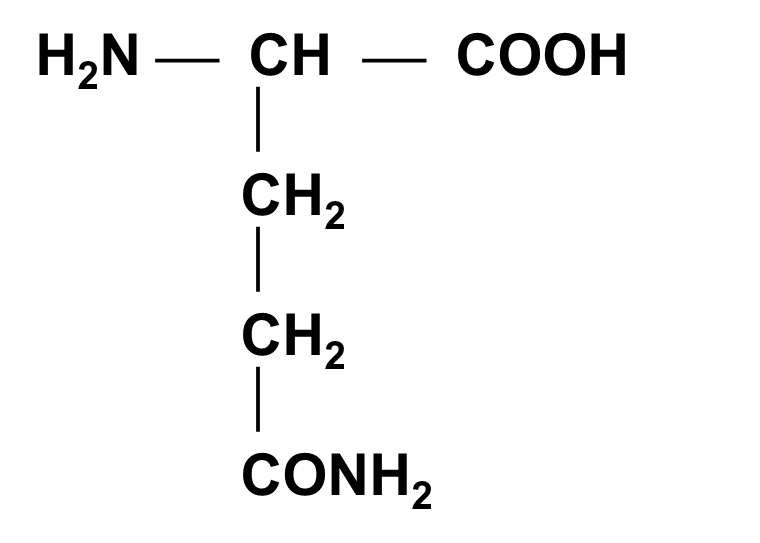
Глутамин (ГЛН)
III. Диаминомонокарбоновые α-аминокислоты (основные)
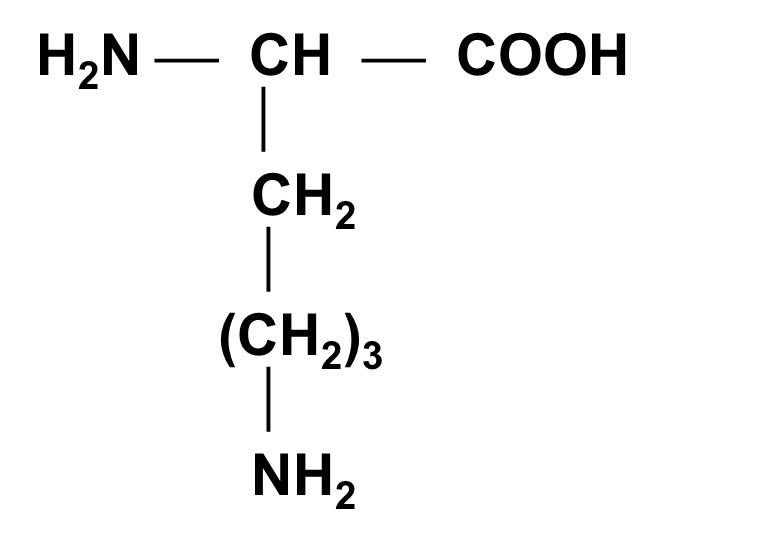
Лизин (ЛИЗ)
A,e-Диаминокапроновая кислота
Боковой радикал гидрофильный, ионогенный, несет положительный заряд (H3N+ ¾ (CH2)4 ¾).
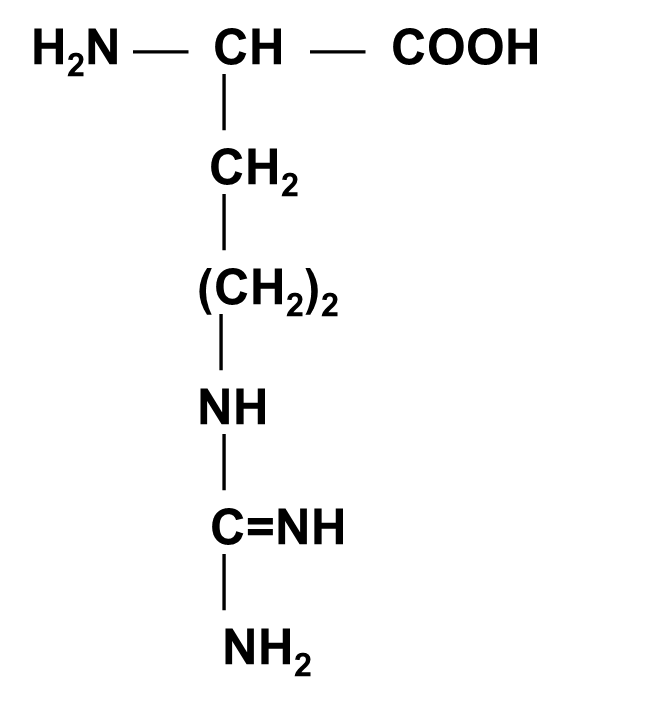
Аргинин (АРГ)
A-Амино-d-гуанидино-валериановая кислота
Боковой радикал гидрофильный, ионогенный, несёт положительный заряд
(H2N+ = C(NH2)¾ NH ¾ ( CH2 )3 ¾).
IV. Оксиаминокислоты
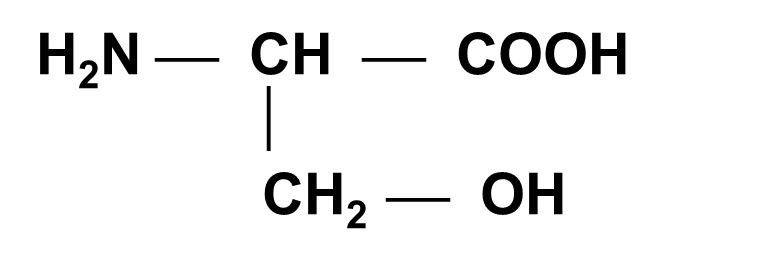
Серин (СЕР)
A-Амино-b-оксипропионовая кислота
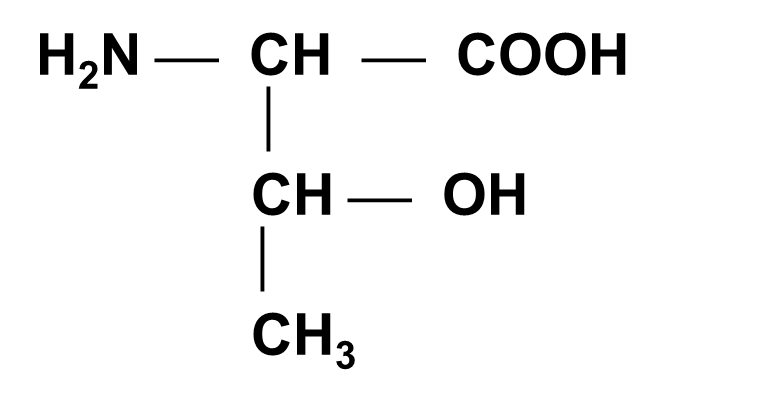
Треонин (ТРЕ)
A-Амино-b-оксимасляная кислота
Боковые радикалы гидрофильные, неионогенные (имеют спиртовую природу).
V. Серосодержащие аминокислоты
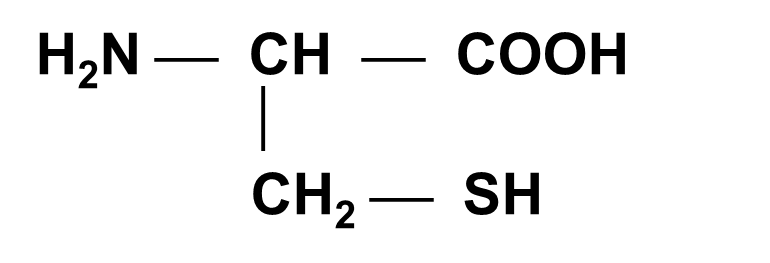
Цистеин (ЦИС)
A-Амино-b-меркаптопропионовая
Боковой радикал гидрофильный, ионогенный, несёт отрицательный заряд
(- S ¾ CH2 ¾).
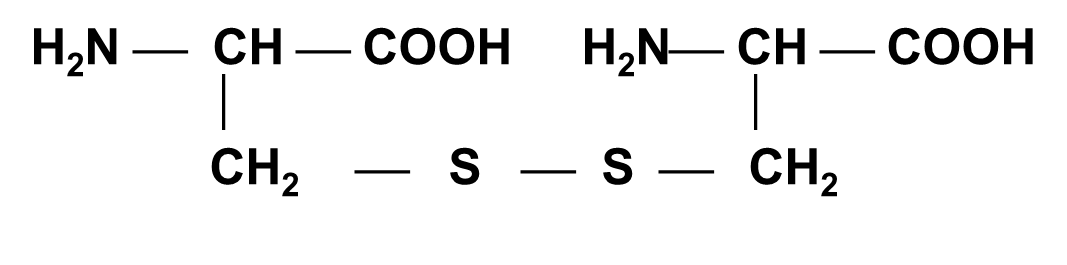
Цистин (ЦИС-ЦИС)
a,a¢-Диамино-b,b¢-димеркаптопропионовая кислота
Боковой радикал гидрофобный.
Метионин (МЕТ)
A-Амино-g-метилтиомасляная кислота
Боковой радикал гидрофобный.
VI. Ароматические a-аминокислоты

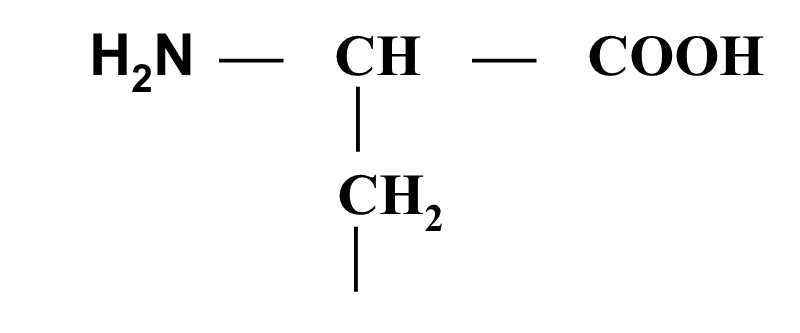
Фенилаланин (Фен)
A-Амино-b-фенилпропионовая
Кислота
Боковой радикал гидрофобный.

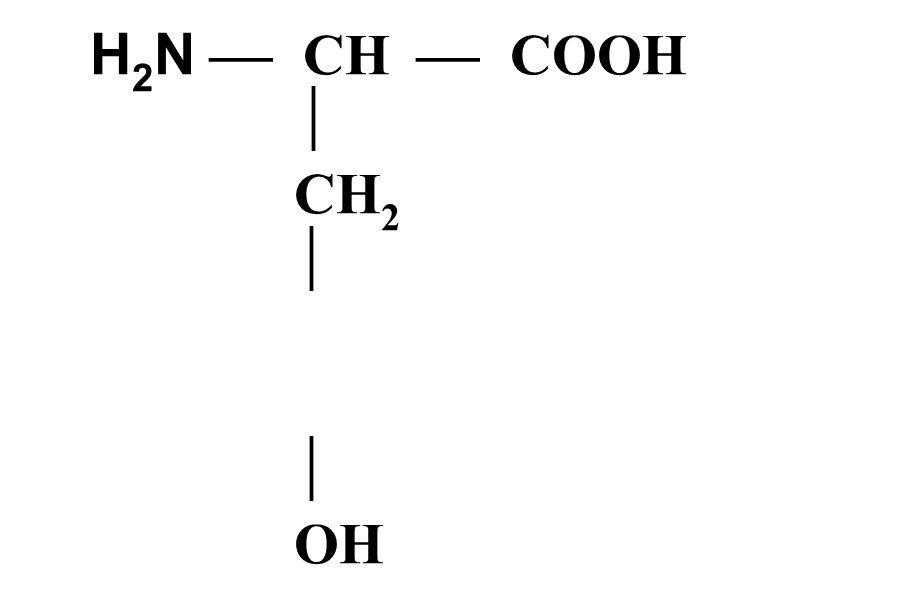
Тирозин (ТИР)
A-Амино-b-параоксифенилпропионовая кислота
Боковой радикал гидрофильный, ионогенный, несёт отрицательный заряд.

VII. Гетероциклические a-аминокислоты
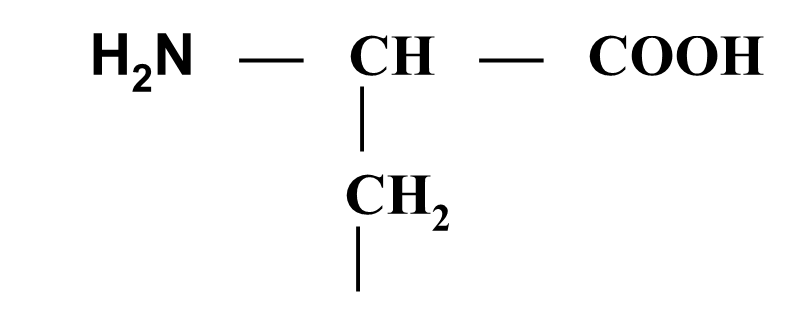
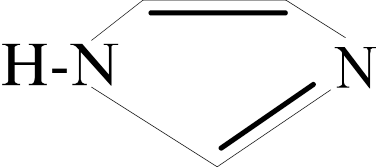
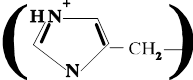
Гистидин (ГИС)
α-Амино-b-имидазолилпропионовая кислота
Боковой радикал гидрофильный, ионогенный несёт положительный заряд
|
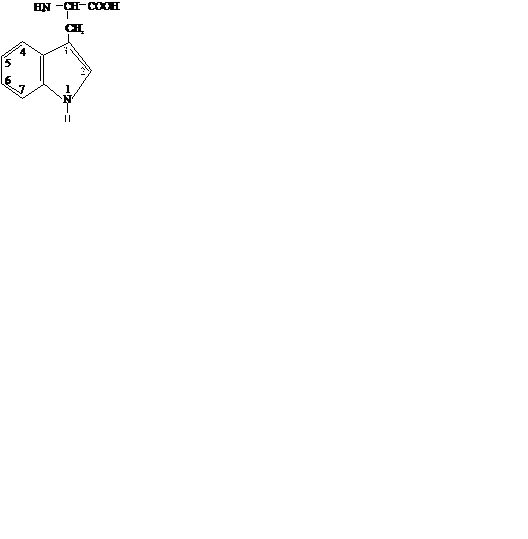
Триптофан (ТРИ)
Боковой радикал гидрофобный, неионогенный.
Иминокислоты
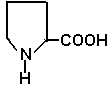
Пролин (ПРО)
Боковой радикал гидрофобный, неионогенный.
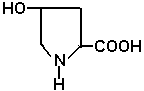
Оксипролин (ОПР )
Боковой радикал гидрофйльный, ионогенный.
Кислотно-основные свойства a-аминокислот
По протолитической теории кислот и оснований, a-аминокислоты относятся к амфолитам, т.к. содержат в составе молекулы кислотный и основной центры. В водном растворе молекула a-аминокислоты существует в виде биполярного иона.

В зависимости от рН среды может преобладать тот или иной заряд.
В сильнокислых средах: (рН=1-2) формируется катионная форма a-аминокислоты. В сильнощелочной среде: (рН = 13-14) преобладает анионная форма a-аминокислоты.

Существуют значения рН спецефические для каждой аминокислоты, в которой количество анионных форм в растворе равно количеству катионных форм. При этом необходимо учитывать наличие ионогенных группировок боковой цепи.
Значение рН при котором общий заряд молекулы a-аминокислоты равен 0, называется изоэлектрической точкой a-аминокислоты(pIАК).
Если рН раствора соответствует изоэлектрической точке a-аминокислоты, то при электрофорезе не происходит движения молекулы в растворе. Если рН раствора<pI, то катионная форма a-аминокислоты движется к катоду. Если рН раствора > pI, то анионная форма a-аминокислоты движется к аноду. На этом основано разделение АК методом электрофореза.
Для большинства белков животного происхождения изоэлектрические точки лежат в пределах от 5,5 до 7,0 (исключение: пепсин – pI = 1, сальмин – pI = 12), т.е. белки обладают более выраженными кислотными свойствами.
При физиологических значения рН = 7,34-7,36 in vivo ни одна a-аминокислоты и ни один белок не находится в изоэлектрическом состоянии, а преобладает анионная форма, отрицательный заряд которой уравновешивается катионами натрия и калия (Na+ и К+).
