Дисперсные системы можно классифицировать по различным признакам:
1. По размеру частиц дисперсной фазы:
первый вариант:
а) высокодисперсные d = 10-9 – 10-7 м (1-100 нм)
б) среднедисперсные d = 10-7 – 10-5 м
в) грубодисперсные d > 10-5 м
предпочитаю давать второй вариант (учебник МГУ):
а) наносистемы (ультрадисперсные) d = 1 - 10 нм
б) высокодисперсные d = 10 нм - 1 мкм
в) грубодисперсные d = 1 - 100 мкм
2. По фракционному составу:
а) монодисперсные
б) полидисперсные
3. По концентрации частиц дисперсной фазы (учебник МГУ):
а) малая
б) большая
4. По характеру распределения фаз (учебник МГУ):
а) сплошное распределение – континуальное
б) сетка тонких прослоек – биконтинуальное
5. По взаимодействию между частицами дисперсной фазы(по кинетическим свойствам)
а) свободно-дисперсные (при малой концентрации дисперсной фазы в жидкой и газообразной дисперсных средах)
б) связно-дисперсные (при большой концентрации дисперсной фазы – биконтинуальное распределение – либо в твердой дисперсионной среде)
6. По взаимодействию между частицами дисперсной фазы и дисперсионной средой:
а) лиофильные - хорошо сольватирующиеся лиофильные дисперсные системы образуются путём самопроизвольного диспергирования, термодинамически устойчивы.
Пример: растворы коллоидных ПАВ (образующих мицеллы при концентрации выше ККМ) и растворы полимеров.
Несмотря на то, что эти системы - гомогенны, тем не менее, они относятся к объектам изучения коллоидной химии, так как размеры агрегатов коллоидных ПАВ и макромолекул полимеров соизмеримы с размерами частиц дисперсной фазы в коллоидных системах, что проявляется в некоторых свойствах этих истинных растворов.
б) Все остальные коллоидные системы - лиофобные – неустойчивые, обладающие избытком поверхностной энергии, получаются путем принудительного диспергирования, в них самопроизвольно идут процессы по укрупнению частиц (коагуляции, разрушения). При слипании таких частиц поверхностная энергия уменьшается. По этой причине в коллоидные системы необходимо добавлять стабилизаторы.
7. По агрегатному состоянию фаз (табл. 1.1)
Таблица 1.1
Классификация коллоидных систем по агрегатному состоянию фаз
| Дисперсионная среда Дисперсная фаза | ж | г (аэрозоли) | тв |
| тв ж г | т/ж: континуальные: малая концентрация -золи (коллоидные растворы с d =1-100 нм), суспензии; концентрированные - пасты, биконтинуальные: гели (концентриров. ) ж1/ж2: эмульсии г/ж: свободнодисперсные – газовые эмульсии связнодисперсные – жидкие пены | т/г: в зависимости от дисперсности: дымы, пыли, порошки ж/г: туманы, облака г/г: - не существуют | т1/т2: композитные материалы, горные породы, сплавы ж/т: растительные клетки, живые организмы г/т: пористые материалы: пемза, хлеб, сыр, твердые пены |
Лекция 2
Физическая химия поверхностных явлений
Межмолекулярные связи
Межмолекулярное взаимодействие может иметь различный характер:
1. химические связи – образуются путем перекрывания электронных орбиталей и потому сугубо специфичны
2. водородные связи возникают между молекулами, содержащими функциональную группу – ОН: кислотами, щелочами, водой и др. веществ -
силикагель - Si – OH H
O O
- Si – OH H
3. Силы Ван-дер-Ваальса(*) (молекулярные связи), действующие между любыми молекулами.
Отличия молекулярных сил притяжения от химических:
а) по величине энергии: Емол= 5 - 50 кДж/моль
Е хим = 80 – 800 кДж/моль
б) молекулярные силы неспецифичны
в) различие по радиусу действия
r хим~ 10-8
r мол > 10-7 см
г) молекулярные силы аддитивны, а химические связи насыщаемы
Молекулярные силы взаимодействия включают в себя:
а) ориентационные силы (Кеезома) (*)
Возникают между полярными молекулами в результате взаимодействия дипольных моментов. Из-за диполь-дипольного взаимодействия молекулы приобретают определенную ориентацию относительно друг друга
Энергия ориентационного взаимодействия сильно зависит от расстояния между молекулами:
Е μˉ1/ μˉ2 = - А1/r6 (2.1)
У полярной молекулы– центр тяжести «+» и «-» зарядов не совпадает (дипольный момент μˉi ≠ 0).
Степень полярности зависит от дипольного момента μˉi. Полярность многоатомных молекул определяется полярностями отдельных связей и их расположением относительно друг друга.
К неполярным неорганическим веществам относятся: элементы, симметрические молекулы газов, некоторые соли (сульфиды металлов).
При рассмотрении полярности или неполярности молекул органических следует обращать внимание не только на наличие полярной группы в молекуле, но и на расположение их в структурной формуле молекулы.
Например:
б) индукционные силы (силы Дебая(*)). Диполь у неполярной молекулы возникает в электрическом поле или под действием поля полярной молекулы.
Энергия связи зависит от поляризуемости молекул и также сильно уменьшается с увеличением расстояния:
Е инд = - А2/r6 (2.2)
в) дисперсионные силы (силы Лондона(*)) действуют между всеми молекулами. Возникают из-за непрерывного движения электронов в атомах, приводящего к образованию мгновенных диполей. В свою очередь электрическое поле мгновенного диполя одного атома индуцирует дипольный момент соседнего, что приводит к возникновению сил притяжения.
Е дисп = - А3/r6 (2.3)
 точнее
точнее 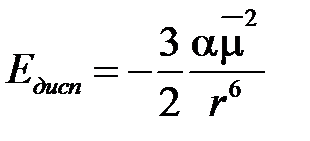 , (2.4)
, (2.4)
где α – поляризуемость молекулы.
Дисперсионные силы притяжения не зависят от температуры.
Молекулярные силы быстро убывают с увеличением расстояния между молекулами.
Рассмотрим соотношения между отдельными силами притяжения молекул (табл. 2.1):
Таблица 2.1
